ÚLTIMA HORA
EN DOLOR
NOTICIAS

ACTUALIZACIÓN EN DOLOR
en el XXVII Congreso
Nacional de la SEMG
Resumen de ponencias más destacadas
Entre los días 14 y 19 de junio tuvo lugar en el Palau de Congressos de Palma de Mallorca el congreso de la Sociedad Española de Médicos Generales y de Familia (SEMG). La situación que ha generado la pandemia obligaba a pensar en un formato adaptado, dando lugar a un congreso híbrido: virtual desde el 14 al 16, y en doble formato (virtual y presencial) desde el 17 al 19 de junio. El evento incluyó todas las actividades habituales: mesas de controversias, talleres, aulas formativas, comunicaciones, foros de actualización, formación en habilidades indispensables en AP, eventos culturales...
A continuación resumimos los aspectos relacionados con el manejo del dolor que fueron tratados en el congreso. También reseñaremos otros temas que, por su actualidad o especial interés, merecen ser destacados.


HOSPITALIZACIÓN A DOMICILIO:
EL HOSPITAL EN CASA
Los servicios de hospitalización a domicilio han sido claves durante la pandemia, pero lo son siempre por su contribución a un tipo de cuidados más humanizados y una prolongada trayectoria en el manejo del dolor en el que se combina el saber de múltiples disciplinas. Un profesional con una dilatada experiencia en esta modalidad de atención nos ofrece sus reflexiones sobre qué significa tener "el hospital en casa".
Entrevista. Dr. Jorge M. Santander López.
Médico Adjunto, Hospital Universitari de la Ribera. Alzira. Valencia.

La situación pandémica ha potenciado el trabajo de las unidades de Hospitalización a Domicilio (UHAD), perfilándose en un futuro como una solución a la medida de una población en curva ascendente de envejecimiento con una esperanza de vida elevada.
El modelo de hospitalización domiciliaria nace en New York en 1.947 cuando el Hospital Guido Montefiore de esta ciudad implantó este sistema de atención médica. En 1.951, el Hospital Tenon de París fue el primero en crear una unidad de hospitalización domiciliaria en Europa.
En nuestro país fue pionero en 1.981, el Hospital Provincial de Madrid (actual Hospital Universitario Clínico San Carlos). A partir de ese momento, la iniciativa ha ido poco a poco poniéndose en marcha en otros hospitales. Así, en 1.983 el Hospital de Cruces (Vizcaya) puso en marcha una experiencia piloto de atención domiciliaria que fue la primera de este tipo dentro de la red gestionada entonces por el Instituto Nacional de Salud (INSALUD). Y le siguieron otros hospitales: Virgen del Rocío en Sevilla y Marqués de Valdecilla en Santander, ambos en 1.984, General Yagüe en Burgos (1.985), Juan Canalejo en La Coruña (1.987), etc.
La situación pandémica ha potenciado el trabajo de las unidades de Hospitalización a Domicilio (UHAD), perfilándose en un futuro como una solución a la medida de una población en curva ascencente de envejecimiento con una esperanza de vida elevada.
Hemos tenido el placer de entrevistar al Dr. Jorge M. Santander que nos habla del presente y futuro de la Hospitalización a Domicilio.
¿Qué es la hospitalización a domicilio y cuáles fueron sus orígenes?
La hospitalización a domicilio nació de la necesidad de descongestionar la asistencia médica en los hospitales, aliviando la presión asistencial “ampliando cama” en la residencia del paciente.
Con el tiempo, las innovaciones tecnológicas y los medios diagnósticos permiten trasladar equipos de alto rendimiento de una forma cómoda y fácil a los domicilios. Hoy en día contamos con ecógrafos portátiles, bombas de infusión continua, dispositivos de presión negativa, entre otros, que nos ayuda a prestar una mejor calidad asistencial a los pacientes en sus domicilios.
¿En qué consiste la HAD?
La asistencia a domicilio es tan diversa como lo son los pacientes a los que tratamos. Habitualmente son pacientes crónicos complejos, pacientes agudos con tratamientos endovenosos, pacientes con úlceras complejas y pacientes paliativos. En general, son pacientes que no necesitan de la infraestructura hospitalaria, pero si demandan un seguimiento asistencial a la medida en domicilio.
¿Cuáles son los beneficios a nivel asistencial?
Al paciente se le brinda una calidad de atención hospitalaria con el respeto a su entorno vital donde el paciente se encuentra más cómodo, potenciando su calidad de vida. Este es el caso de los pacientes añosos que en la asistencia hospitalaria habitual desarrollan problemas de índole psiquiátrica y alteraciones psicoemocionales.
Al paciente se le brinda una calidad de atención hospitalaria con el respeto a su entorno vital donde el paciente se encuentra más cómodo, potenciando su calidad de vida. Este es el caso de los pacientes añosos que en la asistencia hospitalaria habitual desarrollan problemas de índole psiquiátrica y alteraciones psicoemocionales.
Al no sacar a los pacientes de su hogar el proceso de curación es mucho más rápido y satisfactorio. No debemos olvidar los beneficios para familiares y cuidadores.
¿Cómo es el abordaje anímico de estos pacientes? ¿Cómo se gestiona a nivel emocional la comunicación con familiares y cuidadores?
La HAD se plantea al paciente y su entorno como una opción asistencial, por lo tanto, una vez que ellos han elegido este proceso continúan con su asistencia hospitalaria y se sienten respaldados a nivel de cuidados médicos y de enfermería. El nivel de satisfacción es muy bueno.
¿Cómo ha influido la pandemia del COVID-19 en la asistencia domiciliaria?
Ha supuesto un gran cambio en desarrollo de estructuras y en esfuerzo profesional de los miembros de los equipos. Se duplicaron los pacientes domiciliarios y eso nos llevó a una mayor colaboración con dermatología, neurología, neurofisiología, incluso de cirugía general. Aumentamos nuestro trabajo con pacientes con alta precoz y en pacientes paliativos.
¿Ha supuesto la pandemia una potenciación o un mayor conocimiento de la asistencia domiciliaria?
Fundamentalmente ha dejado muy claro la versatilidad de esta unidad. Constituyó desde el principio la primera línea de defensa contra el COVID-19.
En el trabajo del UHAD el paciente paliativo es una realidad prevalente, ¿Cómo se aborda el dolor en este tipo de pacientes?
El dolor en nuestro trabajo diario juega un papel muy importante. En el paciente paliativo la celeridad en diagnosticarlo y tratarlo correctamente es fundamental, ya que la situación del sufrimiento por dolor le hace recordar la situación de los últimos días. Un paciente paliativo con dolor sufre mucho más que un paciente con dolor crónico habitual.
En esto casos diagnosticamos, tratamos y educamos al paciente dándole pautas que mejoren el alivio del dolor y su confortabilidad.
¿Cómo se conforman los equipos para el tratamiento pluridisciplinar del dolor?
En la Unidad de Hospitalización a Domicilio tenemos un estrecho contacto con la Unidad de dolor y en nuestro equipo tenemos a una compañera que desarrolla también su actividad en esta unidad.
¿Cuál es la situación actual de la UHAD y cómo veis el futuro a corto y largo plazo?
La hospitalización a domicilio juega un papel importantísimo, descongestionando la presión asistencial en este proceso de pandemia. El futuro es prometedor ya que se perfila como una solución asistencial relevante ante un rápido envejecimiento de la población, por su versatilidad, por su rápida puesta en funcionamiento, su sostenibilidad dentro del sistema sanitario y la optimización de sus recursos.
Un factor potenciador de la HAD es el cuidado del factor emocional y calidad de vida de nuestros pacientes.



CONGRESO MUNDIAL VIRTUAL SOBRE DOLOR DE IASP 2021

El IASP 2021 es la principal reunión mundial dedicada a compartir nuevos desarrollos en la investigación, el tratamiento y la educación del dolor. Este evento tan esperado reúne a miles de delegados de más de 100 países en múltiples disciplinas. Los participantes incluyen científicos básicos, investigadores, clínicos, médicos, estudiantes y aprendices, todos los cuales están dedicados a mejorar el alivio del dolor en todo el mundo.
La situación de pandemia que atravesamos ha obligado a adaptar el formato de las reuniones científicas a nivel mundial. La IASP también ha debido adaptarse a estos tiempos, transformando su reunión anual. El congreso se ha realizado en dos etapas, del 9 al 11 y del 16 al 18 de junio, en formato virtual. A pesar del cambio de formato, el interés y calidad de los contenidos no ha disminuido.
Después del congreso, Grünenthal ha realizado unos webinars en los que un grupo de expertos nacionales en el campo del dolor, analizan los contenidos más relevantes presentados en la IASP. Los webinars están coordinados por el Dr. Javier de Andrés López, Coordinador de la Unidad de Dolor del Hospital Universitario La Paz, y analizados por los Dres. Gustavo Fabregat Cid, Anestesiólogo de la Unidad Multidisciplinar de Tratamiento del Dolor del Complejo Hospitalario General Universitario de Valencia e Isaac Peña Vergara, Coordinador de la Unidad de Dolor de Hospital Universitario Virgen del Rocío de Sevilla. Sus presentaciones y discusiones están disponibles en la página www.dolor.com, y nosotros ofrecemos aquí un resumen de los puntos clave de esos encuentros.
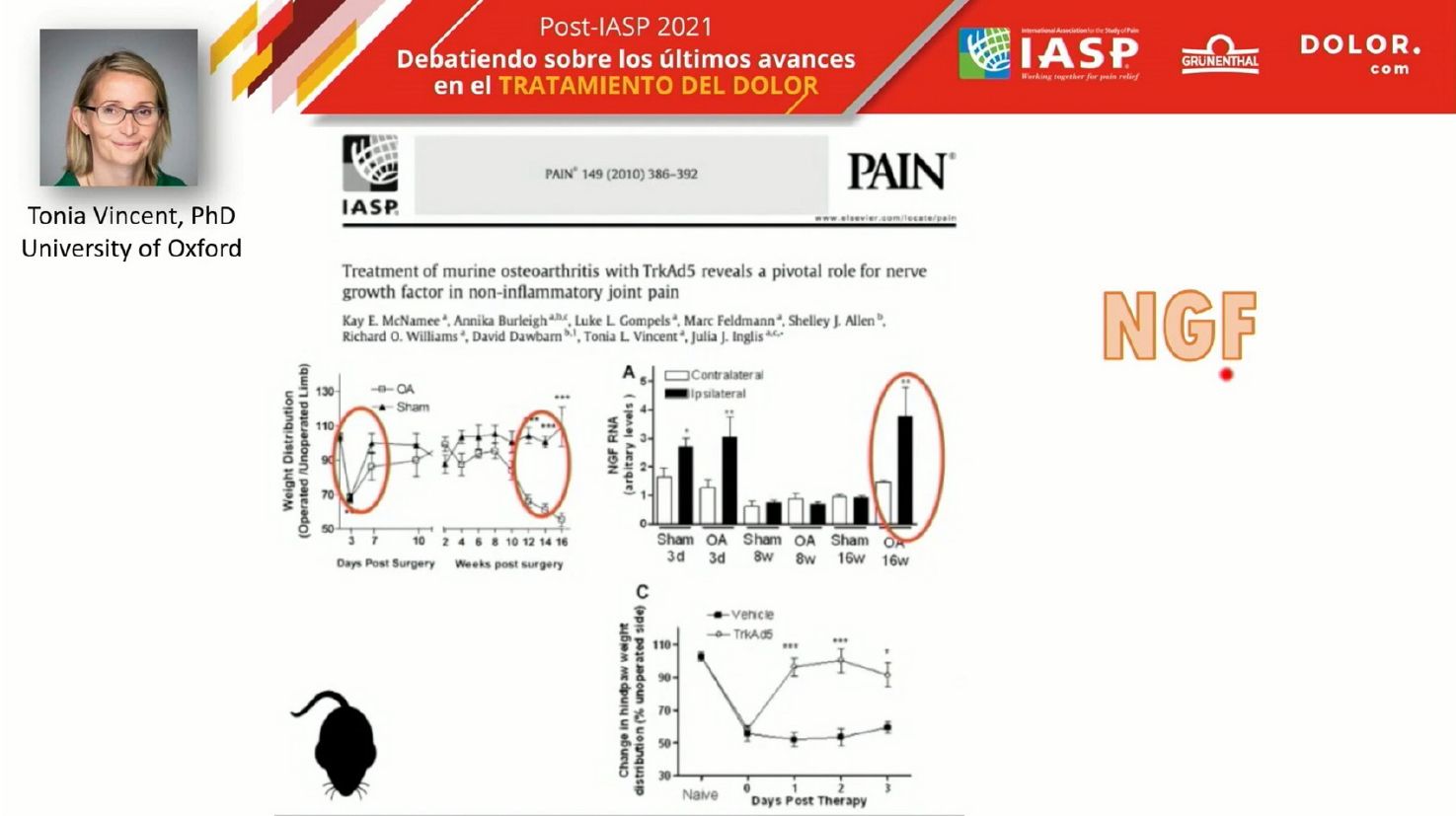
¿ES EL FACTOR DE CRECIMIENTO NEURAL VECTOR DEL DOLOR EN ARTROSIS?
El tema del dolor en artrosis fue presentado en el congreso por la Dra. Tania Vincent, de Reino Unido, y analizado por el Dr. Fabregat, quien comentó que lo más interesante de la ponencia fue la explicación de la patogénesis del dolor en esta condición.
La artrosis es una lesión articular mecánica causada por aumento de carga en una articulación normal o por una carga normal en una articulación que ha perdido los mecanoreceptores por la edad. Por tanto, la patogénesis de la artrosis es bien conocida. El problema radica en que la artrosis afecta al cartílago articular, que no tiene inervación sensitiva, lo que hace difícil explicar que se origine dolor.

Durante años se han usado modelos murinos para intentar encontrar qué moléculas son los vectores del dolor en la artrosis, su causa y su origen titular. Una de las posibles respuestas está en el Factor de Crecimiento Neural (NGF). En el modelo, se tomaron dos grupos de ratones con osteoartrosis quirúrgica y se causó un daño del cartílago articular en un grupo, respetando el otro. A las doce semanas, el dolor quirúrgico se había recuperado en ambos grupos, pero los que tenían daño articular seguían mostrando dolor intenso. Entre las posibles causas se prestó atención al NGF, que estaba incrementado en las articulaciones de los animales que sufrían dolor y se comprobó que el uso de un inhibidor del NGF revertía el dolor.
En la presentación de la Dra. Vincent también fueron interesantes las reflexiones sobre el mecanismo que propone para el desarrollo del dolor en la artrosis: la aparición de fuerzas de cizallamiento sobre el cartílago articular de una articulación normal causan el fisuramiento del cartílago, activando los condrocitos, que empiezan a segregar NGF (junto con otras sustancias). El NGF provoca la migración de nervios desde la zona subcondrial, neoinervando el cartílago calcificado, causando el dolor. La Dra. Vincent propone que el NGF tiene un efecto doble: neoinervación del cartílago y sensibilización de las fibras dolorosas. También intervienen otras moléculas, como el CCL2. La sensibilización molecular por este mecanismo podría ser diferente para hombres y mujeres.
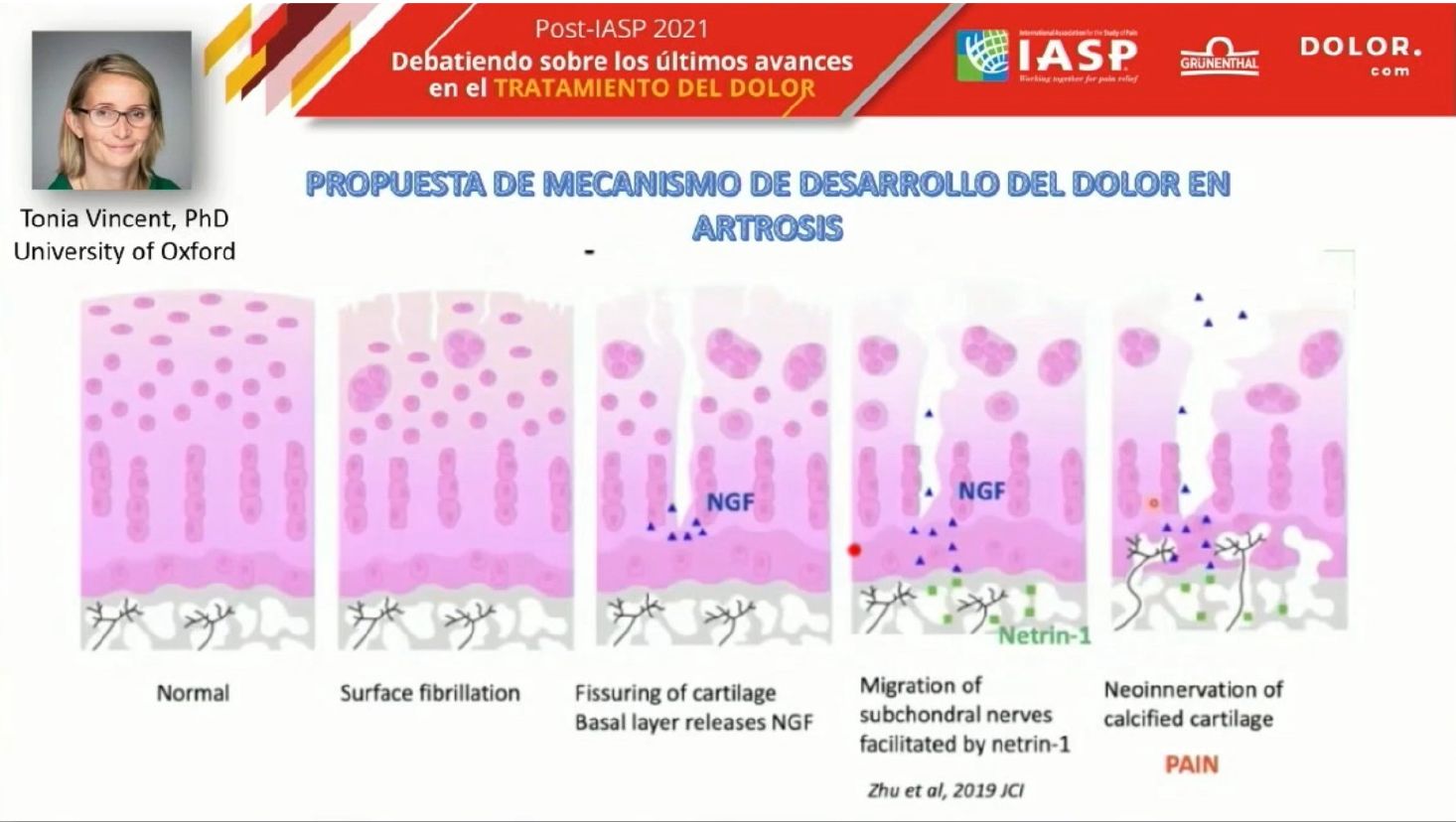
El NGF provoca la migración de nervios desde la zona subcondrial, neoinervando el cartílago calcificado, causando el dolor.
Este modelo podría explicar la falta de correlación entre el deterioro articular y la intensidad del dolor referido por el paciente, que frecuentemente se observa en la clínica.
EL COMPONENTE AUTOINMUNE DE LA FIBROMIALGIA
El Dr. Fabregat también comenta la presentación de la Dra. Camilla Svenson, del Instituto Karolinska de Suecia, dentro de la mesa de Autoanticuerpos y Dolor.
La Dra. Svenson habla de las inmunoglobulinas en fibromilagia, una patología de orígenes físiológicos controvertidos, y considerada principalmente de origen emocional. Para el Dr. Fabregat, el interés de esta presentación es que aporta un nuevo enfoque a las diversas teorías etiopatogénicas de la fibromilagia, reforzando la teoría emergente del posible origen autoinmune.
La propuesta de la Dra. Svenson se origina en un experimento en el que inocularon IgG de pacientes de artritis reumatoide en dos grupos de ratones: uno de ellos positivo para el anticuerpo ACPA y el otro grupo negativo. Comprobaron que el grupo ACPA+ presentaba un aumento de la hipersensibilidad mecánica, sin aparición de inflamación articular, es decir, algo causaba dolor sin inflamación macroscópica.
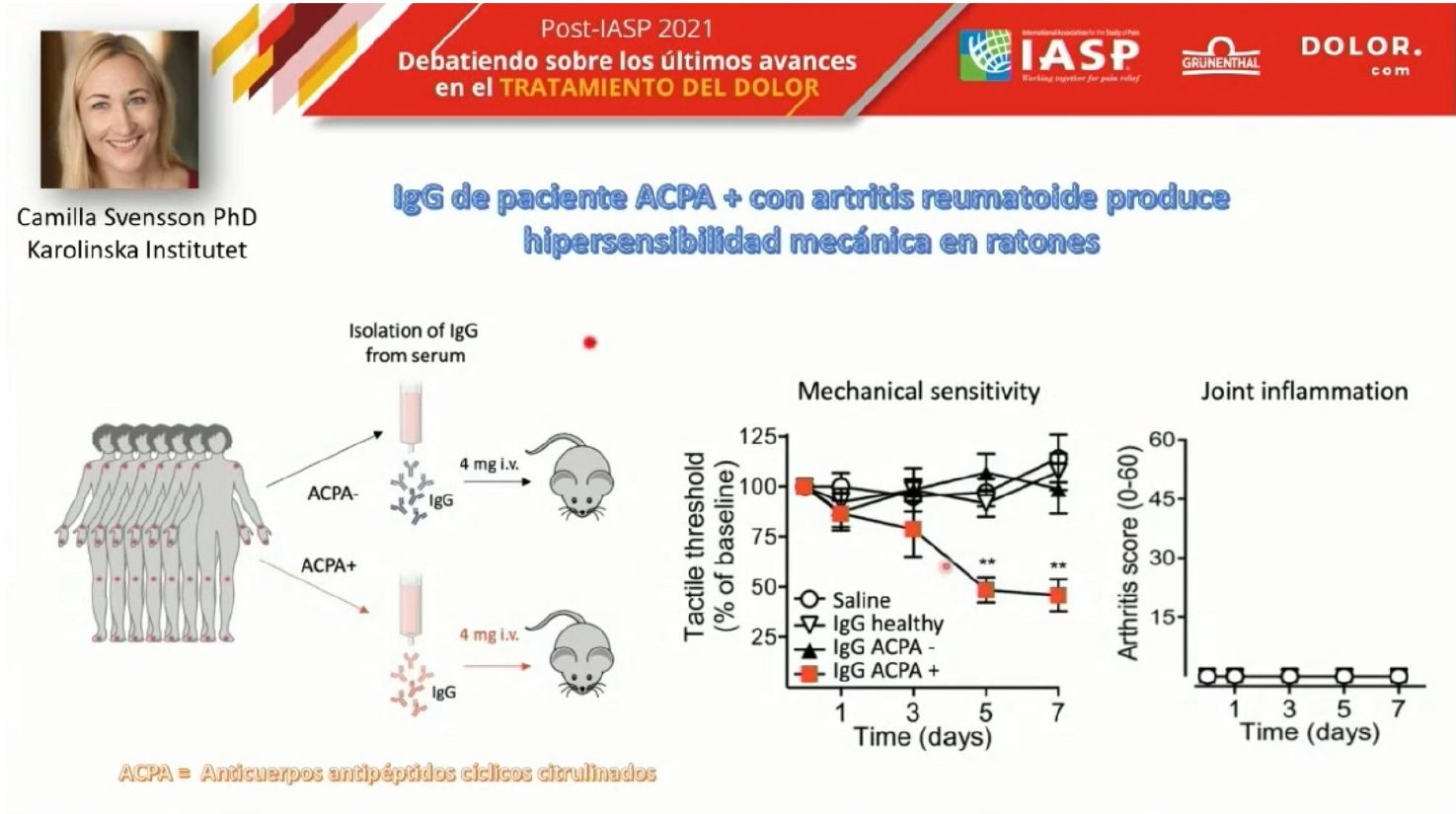
Estos resultados ocasionaron la realización de otro experimento. Se tomó un grupo de pacientes con fibromialgia con altos niveles de dolor y un grupo de pacientes sanos. De ambos grupos tomaron inmunoglobulinas y las inocularon en ratones, obteniendo nuevamente el mismo resultado: los ratones que recibieron las IgG de los pacientes de fibromialgia desarrollaron hipersensibilidad mecánica. Aparecieron además diferencias significativas en la alodinia al frío. Demostraron también alteraciones en los mecanismos nociceptivos y en el comportamiento: los ratones inoculados con anticuerpos de fibromialgia alteraban significativamente su actividad como mamíferos (cuidado de crianza, actividad nocturna…) lo que se interpretó como que sufrían algún tipo de fatiga o cansancio.
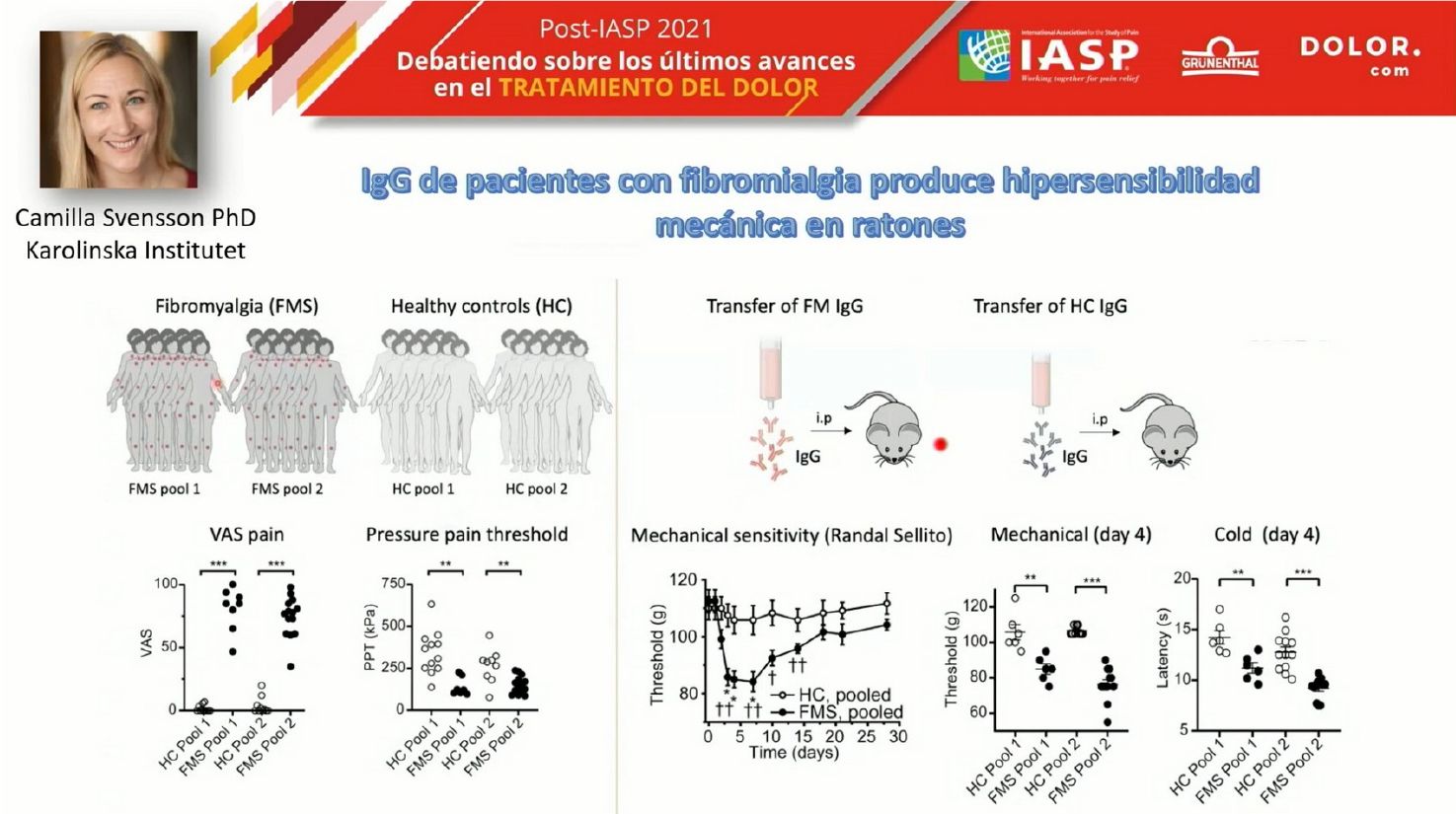
Los ratones inoculados con anticuerpos de fibromialgia alteraban significativamente su actividad.
En estos ratones las IgG se acumulaban en la raíz dorsal y no en otras partes del sistema nervioso central, comprobando además que disminuía significativamente la densidad de las fibras epidérmicas. Es decir, los autoanticuerpos podrían ser mecanismos de generación de fibromialgia, ya que se demostraba que inducen mecanismos y comportamientos asociados al dolor y reducen la densidad de fibras dérmicas.
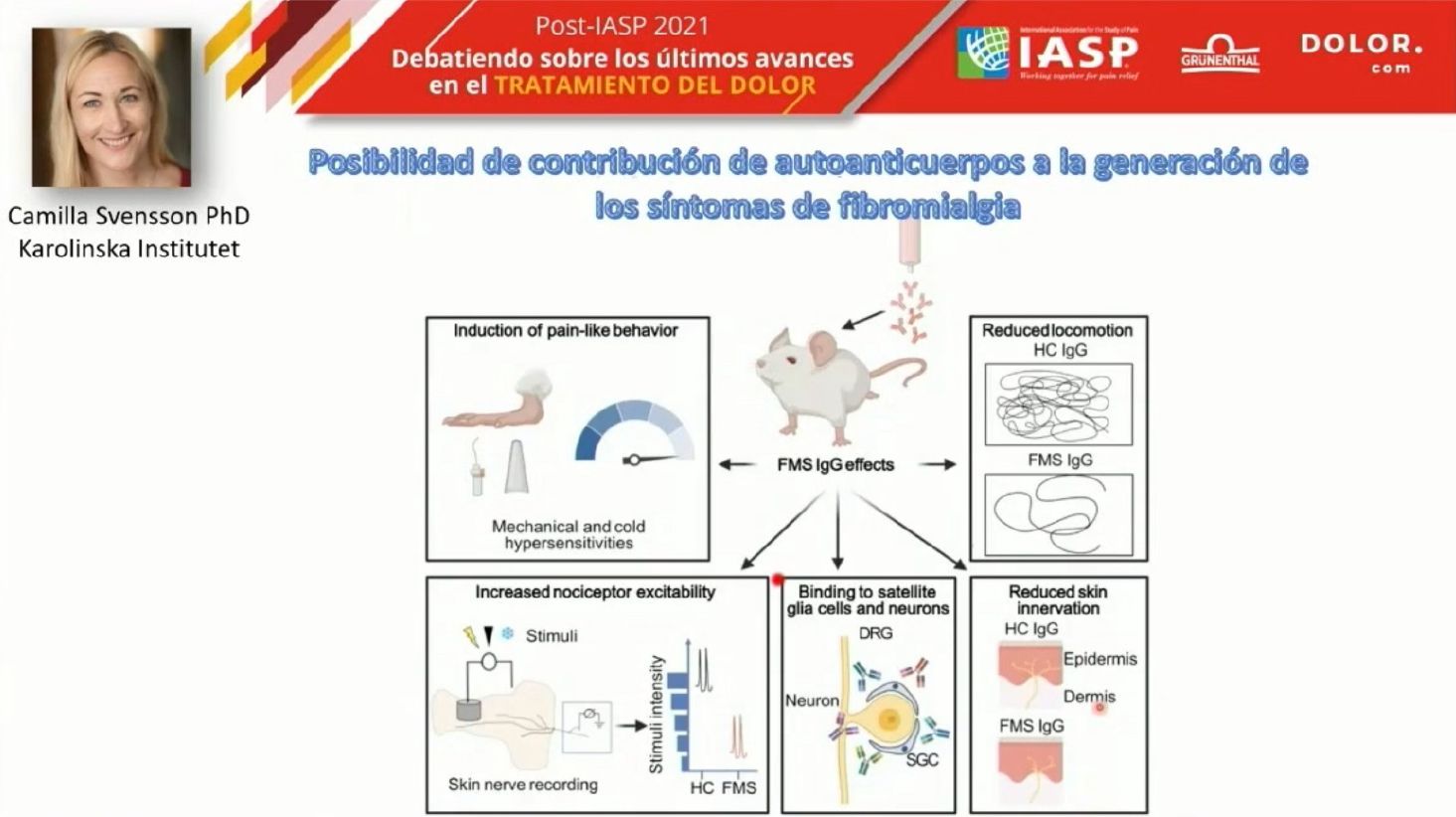
Estos resultados abren la puerta al hallazgo definitivo de una causa objetivable de la fibromialgia, posibilitando la búsqueda de un tratamiento específico en el futuro.
DOLOR RADICULAR: ¿QUÉ HACEMOS MAL CON EL TRATAMIENTO FARMACOLÓGICO?
Nuevamente el Dr. Fabregat resume una presentación muy interesante del Dr. Ralf Baron de la Clínica Universitaria de Scheleswig-Holstein en Alemania sobre la diferencia entre radiculopatía y radiculalgia.
A pesar de las diferencias de la nomenclatura anglosajona y la española, está claro que puede existir radiculopatía sin dolor, es decir, daño en las fibras nerviosas pero que no causa dolor.
Durante la presentación también se intentó dar respuesta a la situación contraria: ¿puede un paciente con radiculopatía presentar dolor lumbar?. El Dr. Fabregat comenta que, cuando existe un mecanismo compresivo sobre una de las raíces, como puede ser un disco, se producen cambios a nivel neuropático y se admite generalmente la presencia de lesiones en los ramos anteriores en las típicas distribuciones metaméricas. Esto provoca alteraciones de sensibilización periférica con aumento de los receptores, y el disparador del dolor lo sentimos siguiendo estas distribuciones metaméricas, compatibles con la afectación de estos ramos.
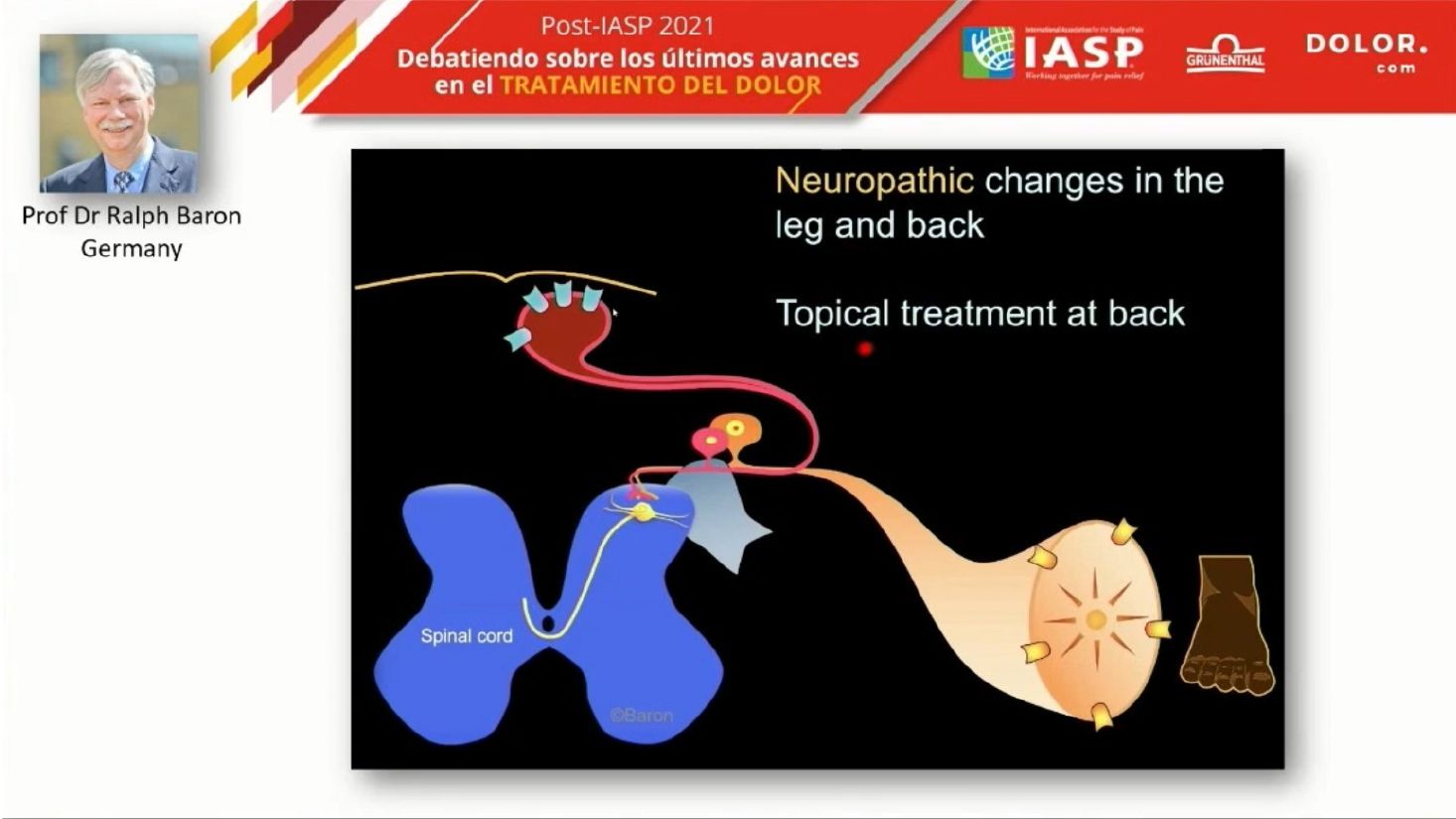
Sin embargo, a la vez que ocurre hacia los ramos ventrales también puede ocurrir con origen en raíces que vienen de los ramos dorsales produciendo los mismos fenómenos de sensibilización periférica dorsal, como vemos en los pacientes con discopatía, en los que aparecen fenómenos de hipersensibilización y de aumento de sensibilización periférica. Por lo tanto, pacientes con radiculopatía pueden tener también dolor en la zona lumbar. Esto podría ser una explicación fisiopatológica de por qué en algunos pacientes con lumbalgia, los tratamientos tópicos contra el dolor neuropático aplicados en la zona lumbar alivian el dolor.
Pacientes con radiculopatía pueden tener también dolor en la zona lumbar.
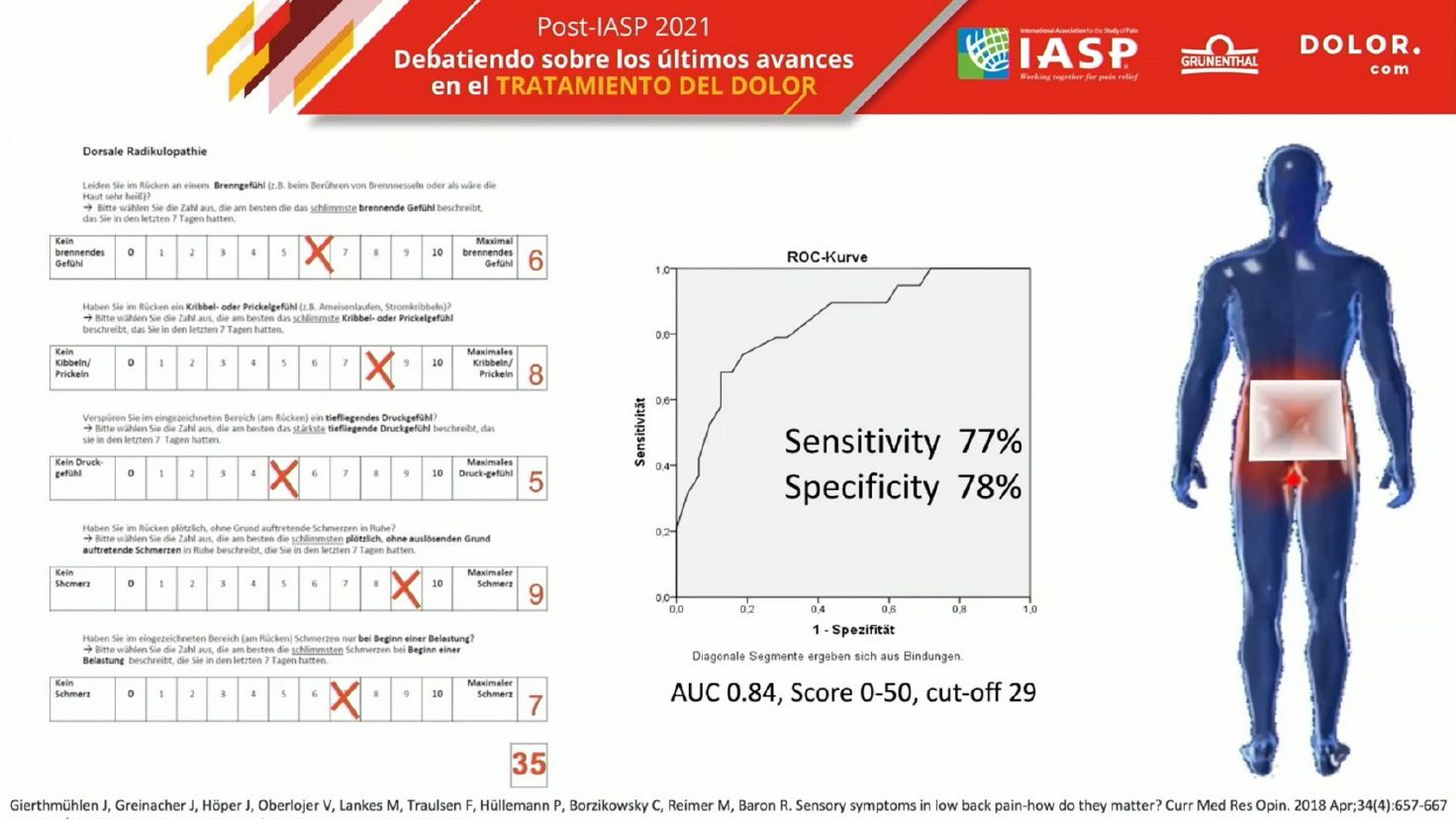
Sería interesante intentar discriminar qué porcentaje de pacientes con radiculopatía la tienen no sólo en los ramos anteriores sino también en la zona lumbar. El Dr. Baron presentó un cuestionario de cinco puntos que ofrece una puntuación final y que busca detectar componentes de dolor neuropático en la zona lumbar de los pacientes con radiculopatía. El cuestionario forma parte de un trabajo publicado hace un par de años que demostró su utilidad en términos de sensibilidad y especificidad, y que puede ayudar en el futuro a ofrecer tratamientos más personalizados a los pacientes con radiculopatía y dolor lumbar. En estos casos, el tratamiento no debe centrarse en tratar las ramas anteriores sino también la zona lumbar.
Todo esto podría explicar los decepcionantes resultados que tenemos con los tratamientos para la ciatalgia, seguramente uno de los dolores neuropático más frecuentes y sin embargo, de los peor tratados. No hay drogas indicadas para la ciática: si repasamos los fármacos para el tratamiento de dolor neuropático que se usan actualmente, vemos que los resultados son poco significativos y no hay tratamiento farmacológico realmente eficaz.
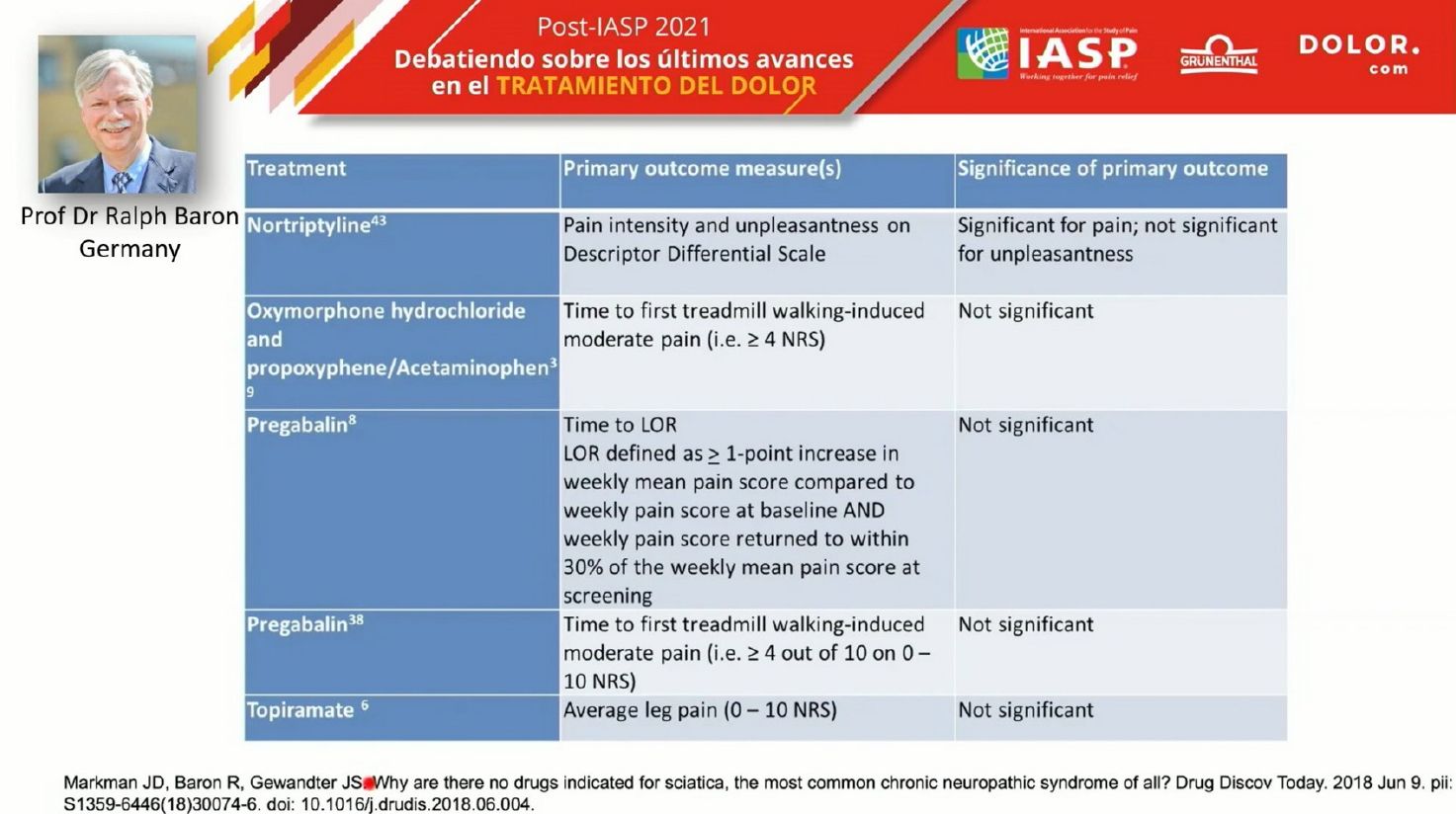
La variabilidad entre pacientes puede ser una causa, por lo que sería recomendable una estrategia personalizada, ya que no todos los que presentan doble radiculopatía o dolor radicular tienen el mismo perfil de dolor neuropático y no todos presentan los mismos mecanismos de dolor neuropático.
El trabajo del Dr. Baron consistió en categorizar a los pacientes utilizando el Pain Predict para seleccionar a pacientes con dolor lumbar y con radiculopatía. De esta forma consiguió establecer una serie de categorías de pacientes en función de los síntomas que predominan: pérdidas sensoriales, hiperalgesia mecánica o sensaciones profundas. Las sensaciones profundas son similares al dolor nociceptivo por eso este tipo de pacientes prefieren tratamientos con AINE y opioides, mientras que otros en los que predomina la hiperalgesia térmica prefieren tratamientos con antipiréticos.
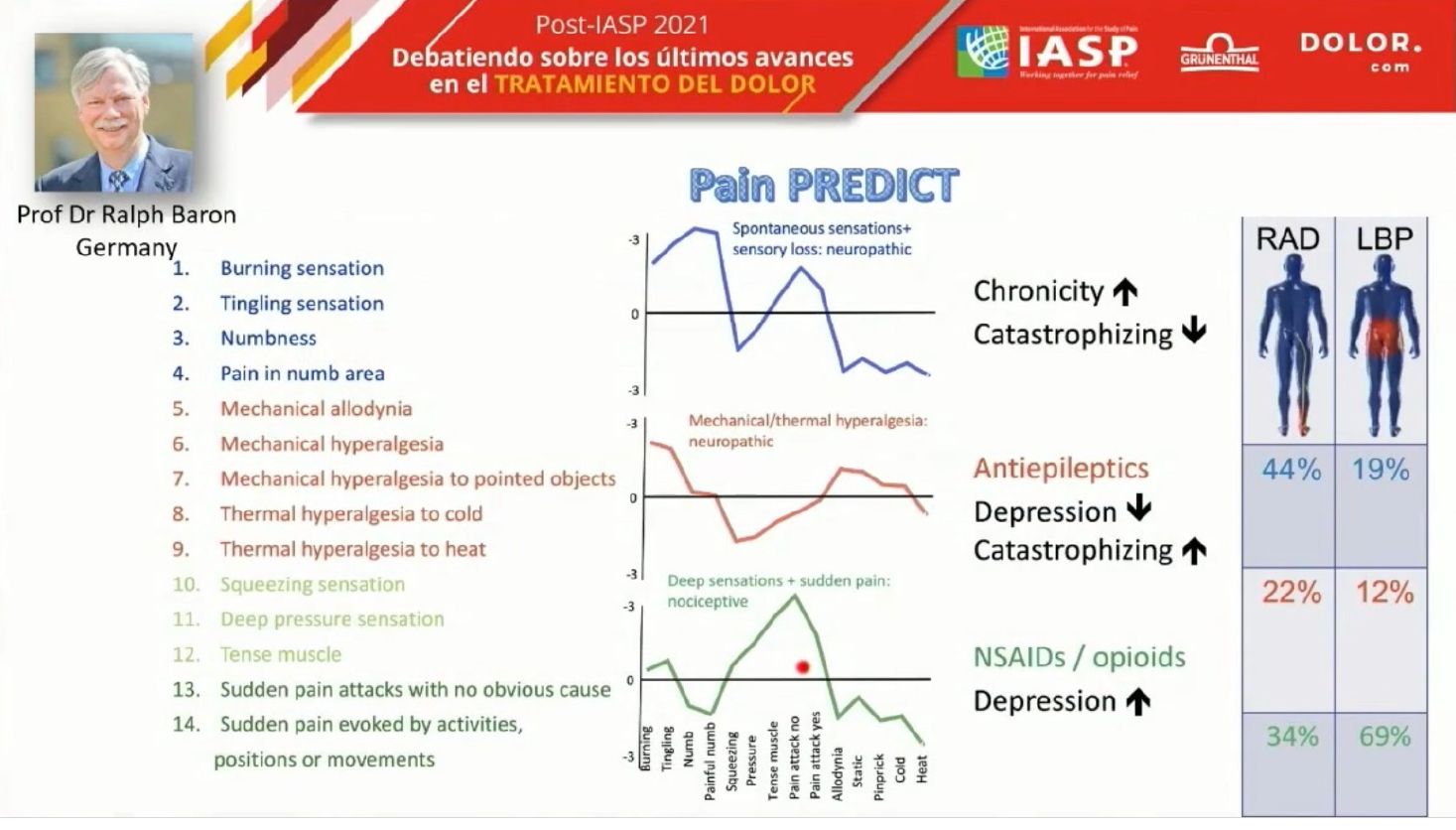
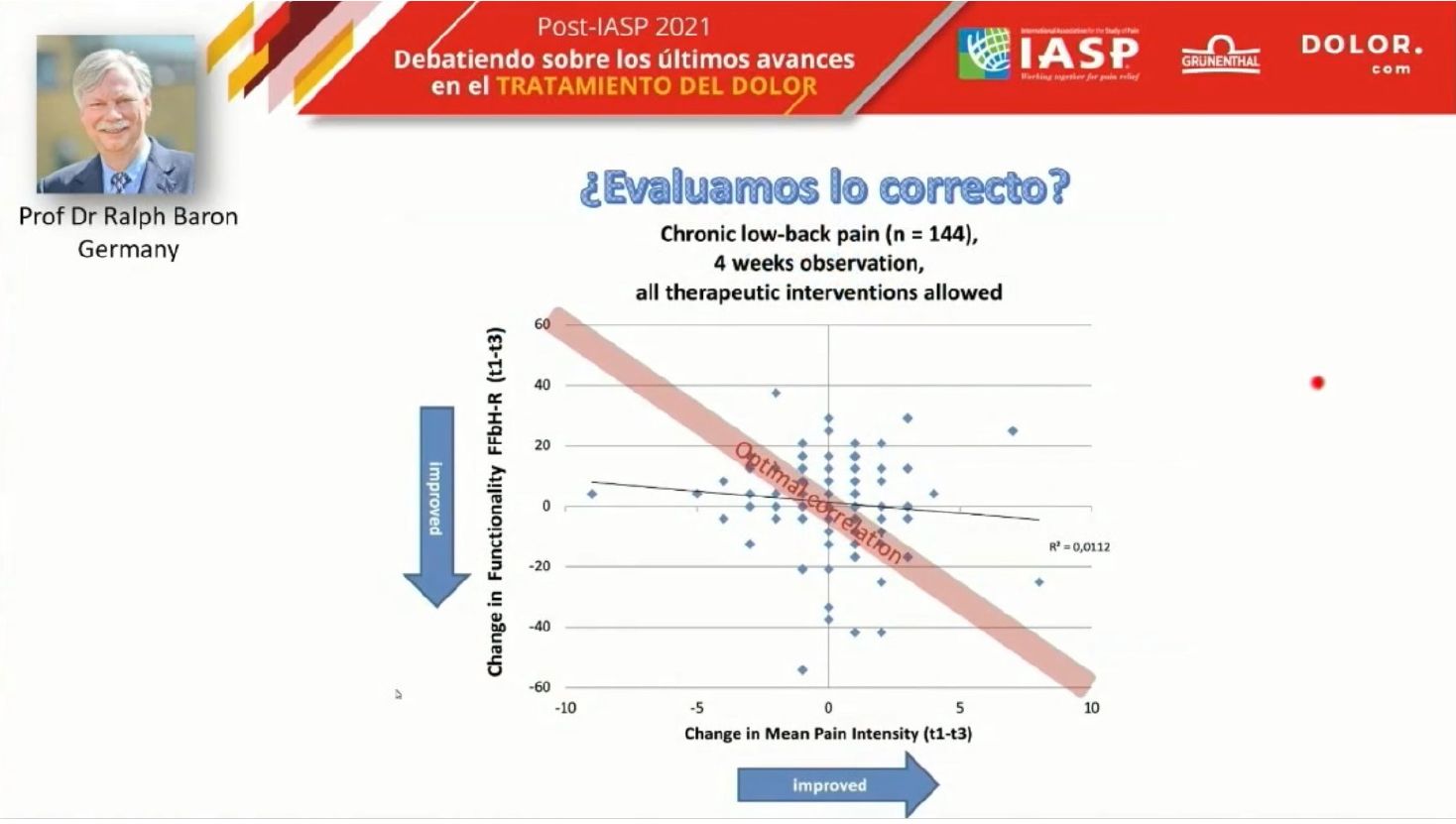
En otro trabajo pendiente de publicación que presentó el Dr. Fabregat, se analiza la relación entre los cambios en la funcionalidad y la intensidad del dolor y se demuestra que no existe una correlación clara entre la mejora en la intensidad del dolor y la mejora en la funcionalidad. Esta falta de correlación sugiere que la medida de la eficacia de los tratamientos del dolor no debe basarse en la reducción de la intensidad del dolor o en la mejora de la funcionalidad.
No existe una correlación clara entre la mejora en la intensidad del dolor y la mejora en la funcionalidad.
El Dr. Ralph Baron comenta que una posible solución sería el uso de los composite outcomes u objetivos o resultados compuestos que, en lugar de basarse en la medición de parámetros, serían en realidad el resultado de combinar otras medidas complejas de la experiencia de dolor del paciente.
Una posible solución sería el uso de los composite outcomes.
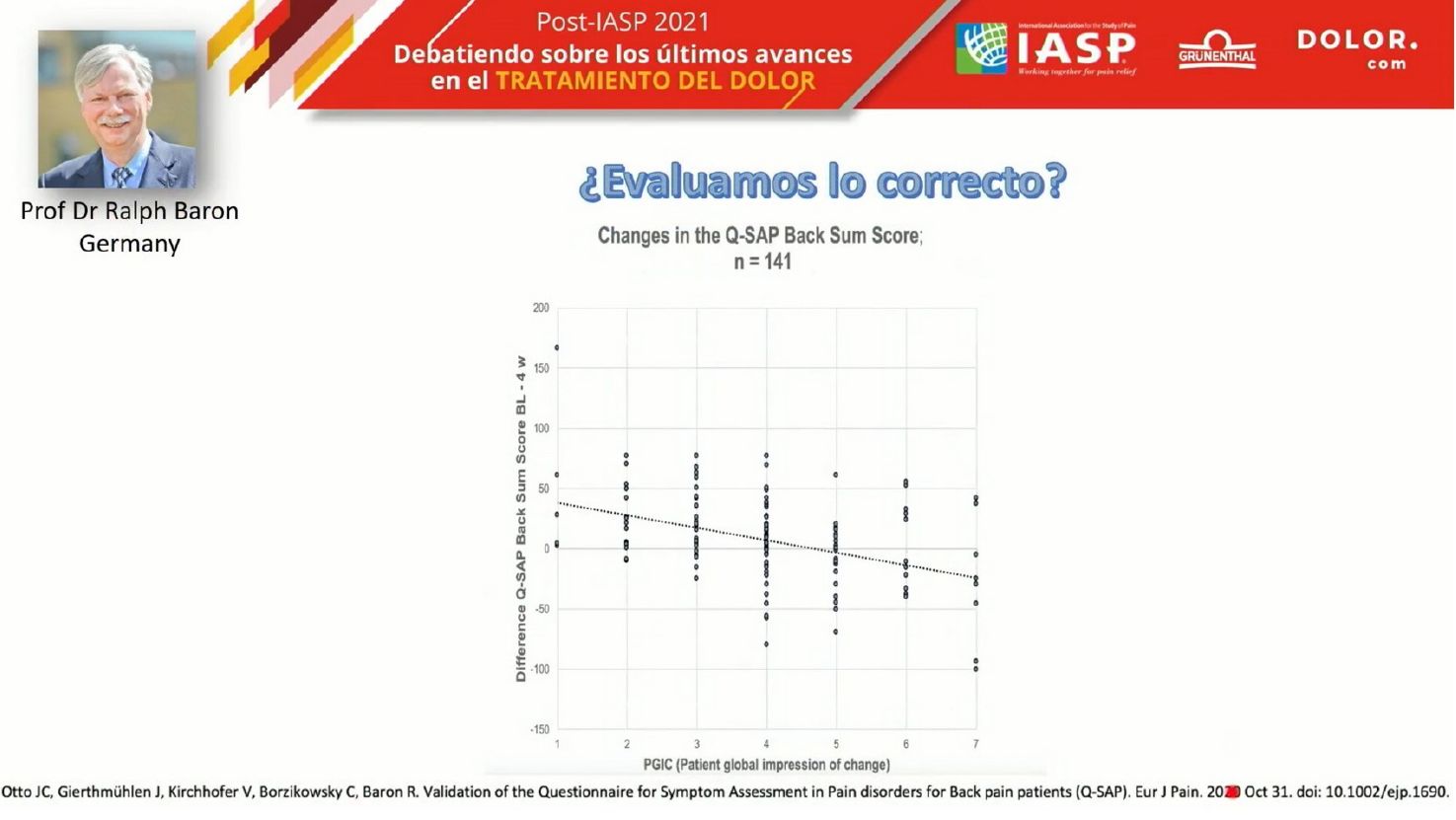
Un ejemplo de esta medición mediante composite outcomes es el cuestionario Q-SAP (Quantitative Symptoms Assessment in Pain Disorders) que presentó el Dr. Baron en IASP. El cuestionario evalúa 12 síntomas diferentes, la intensidad de cada uno, su impacto en la funcionalidad, y su impacto en la calidad de vida, produciendo la combinación de todos ellos una puntuación compuesta. Este cuestionario ha sido validado para el dolor lumbar y se ha comprobado que se correlaciona muy bien con los cambios que percibe el paciente en relación a los tratamientos recibidos. Para el Dr. Fabregat, el uso de este tipo de herramientas puede ayudar a comprender el tipo de dolor que presenta el paciente, permitir ofrecer un tratamiento personalizado y contribuir a desarrollar tratamientos más eficaces para cada tipo de dolor.
FUNCIONALIDAD FÍSICA Y EMOCIONAL EN LOS ESTUDIOS DEL DOLOR
Los Dres. Jennifer Gewander de la Universidad de Rochester en EEUU y Wenlong Huang, de la Universidad de Aberdeen en Reino Unido, presentaron un taller sobre la evaluación de la intensidad del dolor, y la funcionalidad física y emocional como objetivos primarios en los estudios de dolor. El Dr. Fabregat resumió el taller para el webinar.
En el congreso de la IASP hubo dos temas centrales que impregnaban la mayoría de las ponencias: el abordaje holístico del dolor y la necesidad de reenfocar la evaluación del dolor en los pacientes. En este último aspecto, varias ponencias tocaron el tema de los composite outcomes, la medición de resultados complejos, como mejor aproximación para comprender el dolor de los pacientes y personalizar el tratamiento.
Varias ponencias tocaron el tema de los composite outcomes, la medición de resultados complejos, como mejor aproximación para comprender el dolor
El taller comenzó exponiendo que existe una diferencia importante entre las investigaciones clínicas y los fármacos que finalmente están disponibles. Para el primer ponente del taller, el Dr. Huang, el problema podría estar en que los estudios con animales utilizan diversas técnicas para inducir dolor y medir su intensidad, es decir, se basan en la medición de la nocicepción, y en estas medidas se basa la evaluación de la eficacia de los fármacos estudiados. Sin embargo, en los seres humanos existen otros factores, que desde hace años recomiendan un abordaje holístico y multidimensional.
El Dr. Huang considera que, en los trabajos experimentales con animales también hay que incluir otras esferas que influyen en el dolor. Por ejemplo, cada vez se incluye más la medida de las actividades que realizan los roedores en su vida normal y que, si se alteran, indica que están en un ámbito patológico. Una actividad sería la necesidad de excavar, otra sería la tigmotaxis, o curiosidad y necesidad de exploración. Los ratones enfermos presentan alteraciones de estos comportamientos.

En los trabajos clínicos, lo que determina si un tratamiento es eficaz o no, suele ser exclusivamente la intensidad del dolor. Con seguridad, los resultados serían diferentes si incorporáramos más de un dominio en las mediciones, porque hay muchos aspectos que son muy importantes en la vivencia que el paciente tiene del dolor, no solo la intensidad del dolor o la funcionalidad sino también la función emocional, la presencia de efectos adversos, etc.
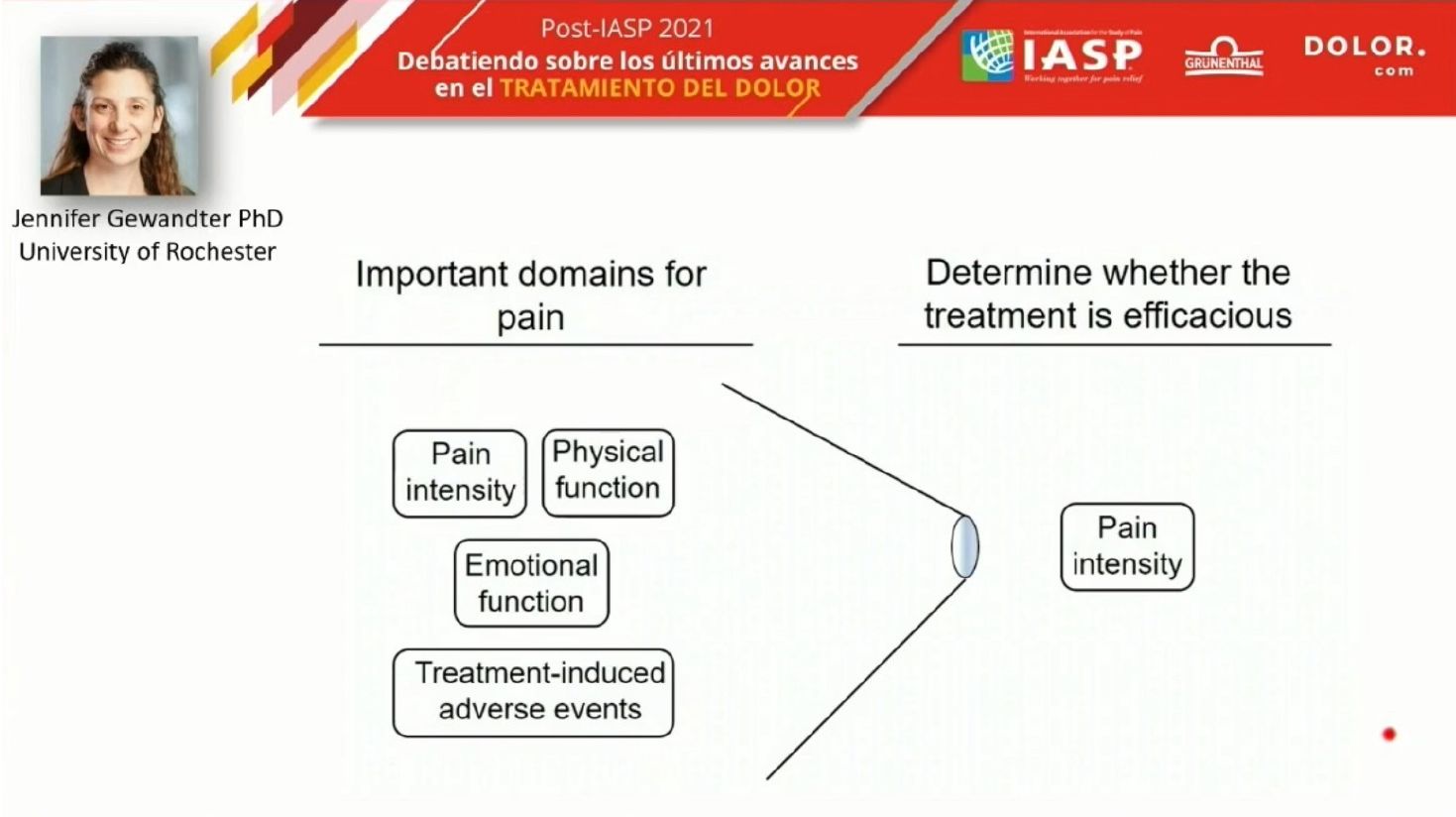
La Dra. Gewander, por su parte presentó un taller práctico con varios ejemplos sobre por qué es necesario medir resultados compuestos en los pacientes. Comenzó presentando un cuadrante en el que el eje x representaba la mejoría de la funcionalidad y el eje y la mejoría en la intensidad del dolor. Por supuesto, el cuadrante inferior izquierdo representaba el peor de los resultados, ya que no se había obtenido mejoría de la funcionalidad ni de la intensidad del dolor. Por otra parte, el cuadrante superior derecho representaba el resultado óptimo, con control del dolor y mejoría de la funcionalidad.
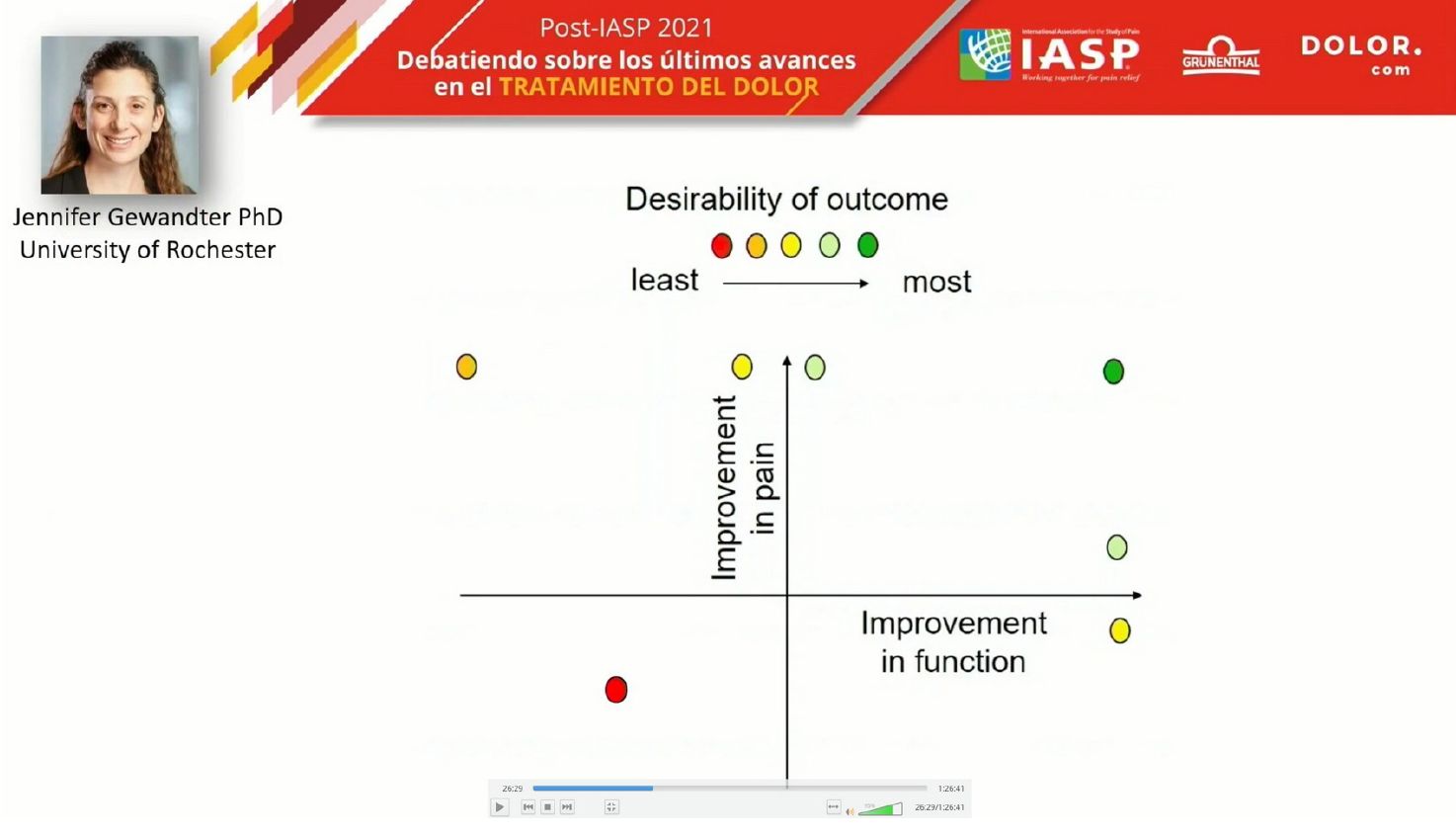
La limitación de esta aproximación es que, cuando medimos sólo un parámetro, por ejemplo, la intensidad del dolor, todos los pacientes que mejoren en intensidad serán considerados iguales, aunque su vivencia del dolor en términos de funcionalidad sea diferente.
De igual manera, también puede darse el caso en que pacientes con igual mejora de la funcionalidad no hayan obtenido una mejoría igual en la intensidad del dolor. En ambos casos, no estamos evaluando correctamente la situación real de los pacientes.
Desde el punto de vista experimental, esto es muy importante, pues un fármaco puede ser muy eficaz frente al placebo en reducción de la intensidad del dolor, pero tener un perfil desfavorable en cuanto a efectos adversos y deteriorar la funcionalidad del paciente. Si sólo evaluamos la eficacia, se trata de un fármaco de éxito, pero pierde utilidad cuando evaluamos otros parámetros en conjunto.
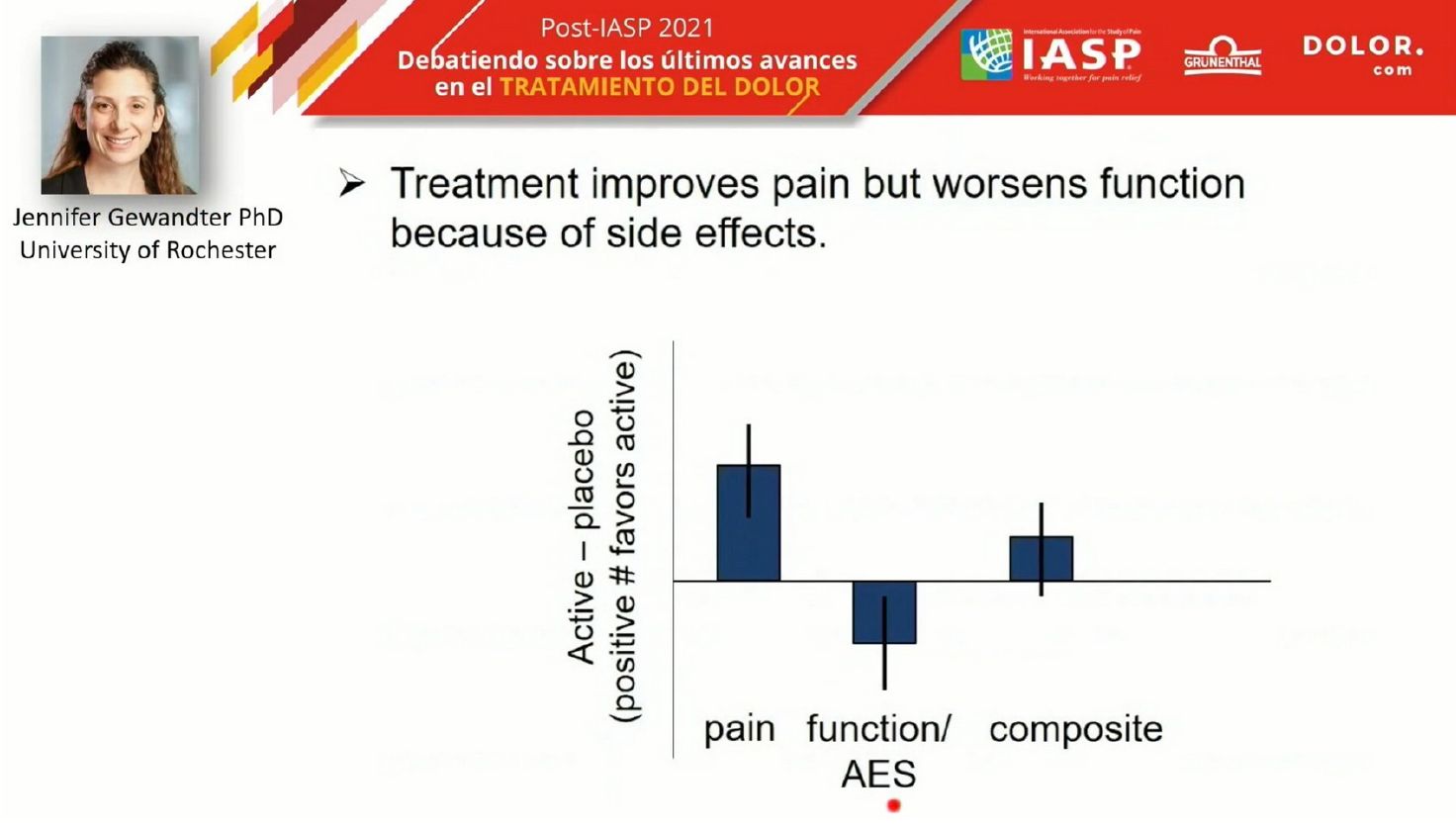
Un fármaco puede ser muy eficaz frente al placebo en reducción de la intensidad del dolor, pero tener un perfil desfavorable en cuanto a efectos adversos y deteriorar la funcionalidad del paciente.
El ejemplo contrario sería el del fármaco que, por su eficacia permite que el paciente reanude su actividad pronto. Sin embargo, al aumentar la actividad puede aumentar el dolor. Tenemos un paciente más activo, pero con algo de empeoramiento en el dolor. Si sólo medimos la eficacia analgésica, el tratamiento no sería útil, a pesar de que el paciente está más activo. Al incorporar la combinación de eficacia analgésica y mejora de la funcionalidad, evidentemente este tratamiento es favorable para el paciente.
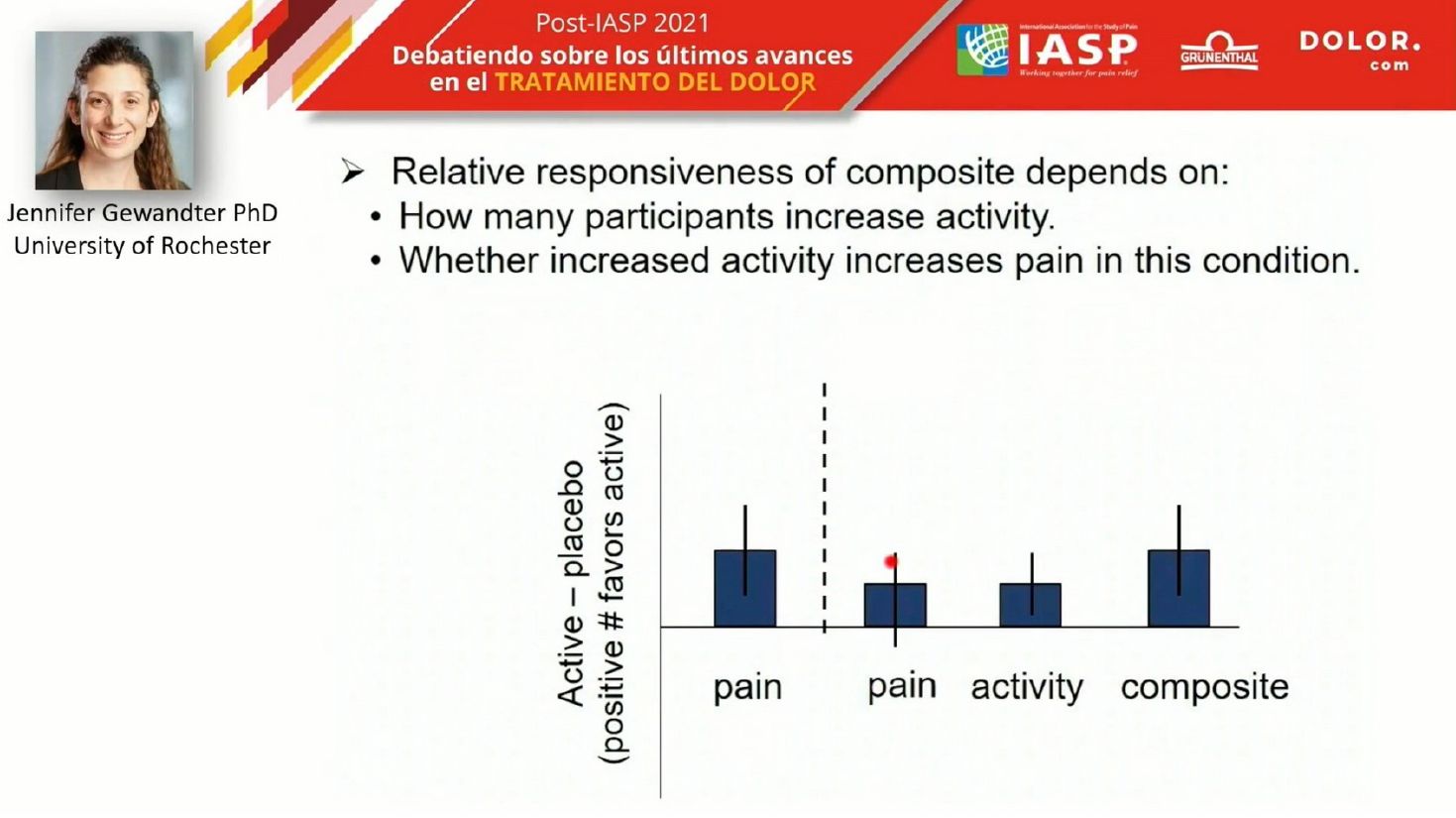
En conclusión, la medida de la eficacia de un tratamiento no debe limitarse a la intensidad del dolor, hay que medir otros parámetros que informen de la mejora en la vivencia del dolor por parte del paciente, como puede ser la mejora de la funcionalidad física y emocional. Los composite outcomes permiten compensar los cambios en diversos dominios de la experiencia del dolor del paciente para ofrecernos una imagen más clara del impacto del tratamiento.
XI REVISIÓN DE LA CLASIFICACIÓN INTERNACIONAL DE ENFERMEDADES (ICD-11)
El Dr. Peña comenta la revisión número 11 de la clasificación internacional de enfermedades. En el congreso de IASP se presentó lo relativo al dolor.
En cuanto al dolor crónico, la actualización la ha realizado un grupo de trabajo liderado por el Dr. Treede, y lo define como aquél de duración superior a 3 meses. También establecen 7 categorías de dolor crónico. El primario es aquel en el que hay un impacto funcional o psicológico tal que constituye por si mismo una patología. Las otras 6 categorías corresponden a dolor crónico secundario causado por una patología conocida y en tratamiento.
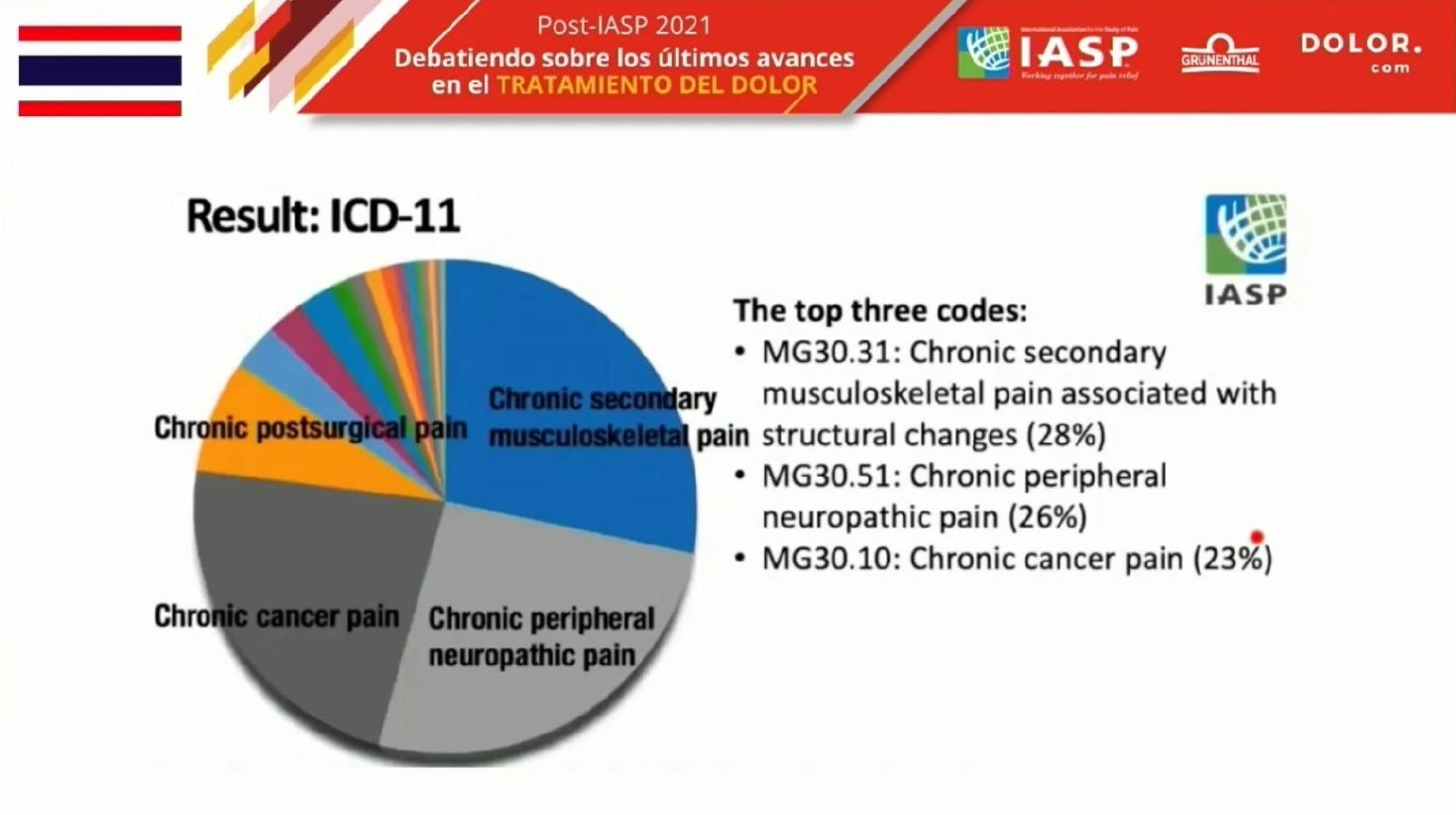
El 98% de los pacientes se puede catalogar fácilmente siguiendo estos criterios.
La utilidad de esta nueva clasificación se ha evaluado en trabajos en todo el mundo y se ha comprobado que el 98% de los pacientes se puede catalogar fácilmente siguiendo estos criterios. Además, el 97% se cataloga sólo en un grupo, lo que da idea de la claridad y especificidad de los criterios de clasificación. Cuando se comparó con la clasificación anterior (IDC-10) se comprobó que el número de pacientes que finalmente se clasificaban con “otros” era mucho más reducido. La gran mayoría de los pacientes tenían un código claro asignado.
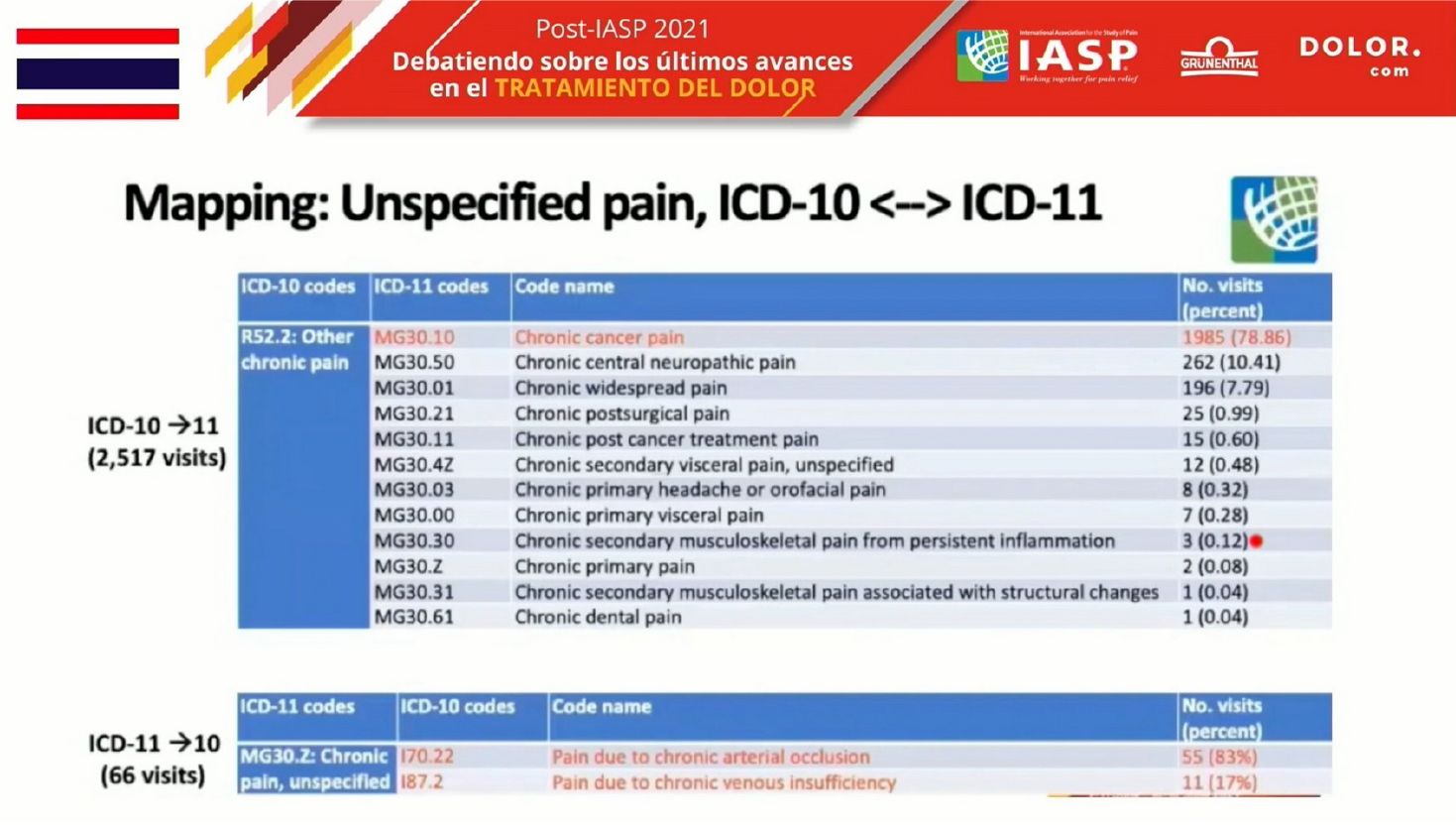
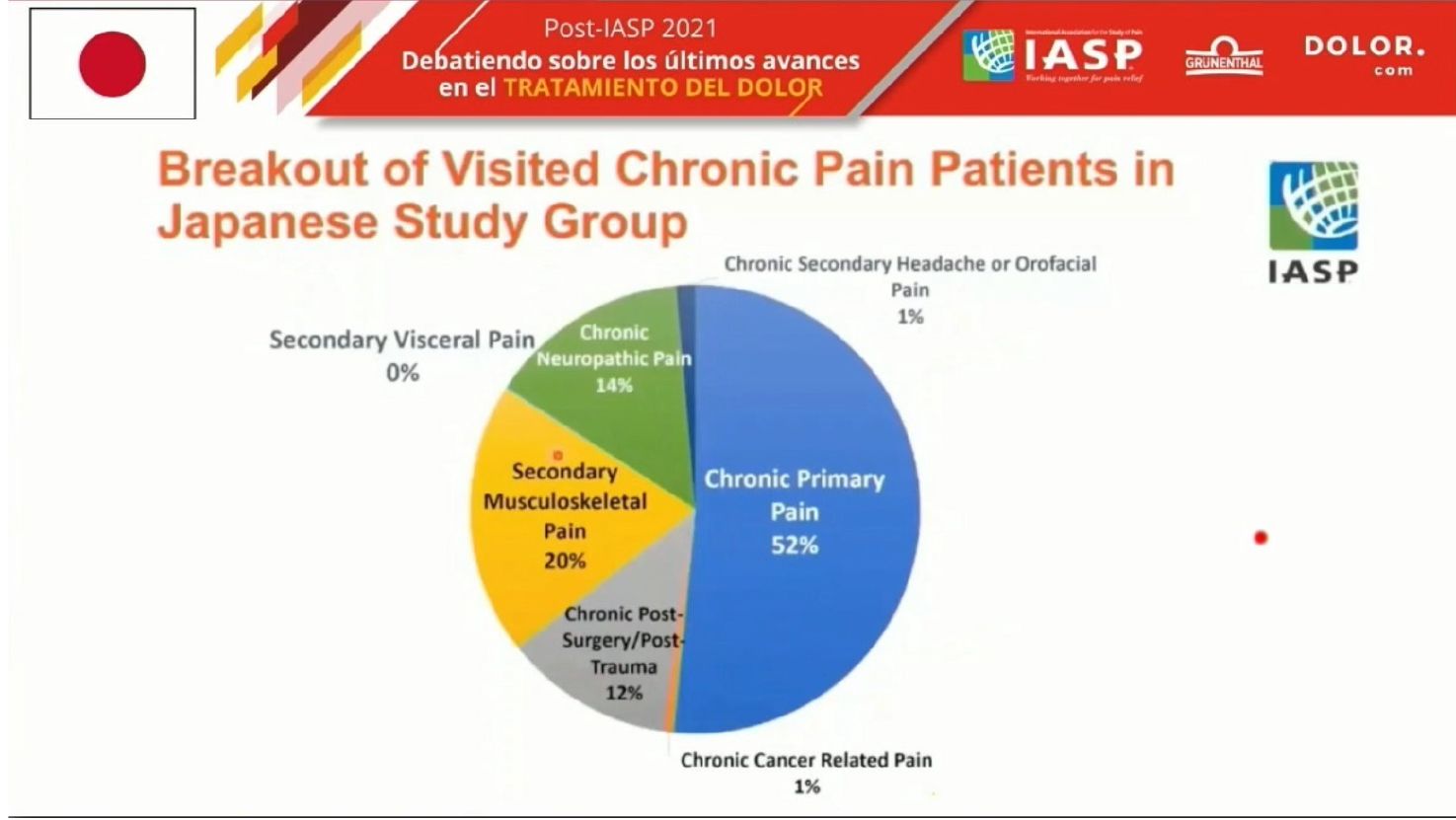
Sin embargo, la evaluación realizada por un grupo japonés mostraba que más de la mitad de los pacientes eran incluidos en el grupo de dolor crónico primario, lo que restaba validez al modelo desde su punto de vista. También presentaron interrogantes en cuanto a la clasificación de los pacientes pediátricos.



LA ADHERENCIA A LOS TRATAMIENTOS DE DOLOR CRÓNICO EN ESPAÑA
La adherencia al tratamiento sigue siendo en nuestra sociedad un problema que va más allá del control o curación de una patología. Son muchos los factores implicados en este fracaso terapéutico que además de producir insatisfacción en el paciente supone una merma de la calidad asistencial y costes al sistema.
El Observatorio del Dolor es una organización vinculada a la Universidad de Cádiz, que tiene por objetivo conocer y difundir la situación del dolor en nuestro entorno social(1). Mediante la realización de encuestas sobre muestras representativas de la población española y/o grupos especiales de población, genera un sistema de información específico sobre las opiniones sobre dolor para, a continuación, difundir los resultados en informes específico (1).
En noviembre de 2020, el Observatorio del Dolor publicó en la revista científica Journal of Clinical Medicine los resultados de un estudio realizado en España: “A nationwide cross-sectional study of self-reported adherence and factors associated with analgesic treatment in people with chronic pain” (Estudio transversal nacional de adherencia autorreportada y factores asociados con el tratamiento analgésico en personas con dolor crónico)(2). En este trabajo, encontramos datos muy interesantes sobre la adherencia que los pacientes de dolor crónico españoles tienen a los tratamientos de dolor(2).

La publicación de este informe vuelve a poner de actualidad el problema de la adherencia a los tratamientos y más concretamente a los tratamientos para el dolor crónico. Aprovechando su publicación, repasamos aquí algunos aspectos de este complejo problema.
La adherencia: la barrera hacia la eficacia
Desde hace algunas décadas, el cuidado de los pacientes ha pasado de estar enfocado en el manejo de la enfermedad a enfocarse en la mejora de la calidad de los tratamientos(3). La falta de adherencia es un obstáculo desde este punto de vista.
Según la Organización Mundial de la Salud, la adherencia a las terapias de larga duración se define como “el grado en el que el comportamiento de una persona que toma una medicación, sigue una dieta o realiza cambios en su estilo de vida, se corresponde con las recomendaciones acordadas con su médico”(4–6). Este término de uso común implica que el paciente tiene un papel activo en el manejo de su enfermedad(7).
En el otro extremo, la falta de adherencia a la medicación se define frecuentemente como tomar menos del 80% de las dosis prescritas, o tomar más dosis de las recomendadas. La falta de adherencia se asocia a un mayor riesgo de mala salud, efectos adversos y mortalidad(2,6).
En los países desarrollados, la adherencia de los pacientes con enfermedades crónicas es de sólo entre el 40% y el 50%(4–6). Es decir, sólo toman aproximadamente la mitad de sus dosis, y muchos de ellos abandonan el tratamiento por completo(7). En las enfermedades crónicas, las intervenciones terapéuticas requieren un compromiso especial por parte de los pacientes, que además quieren comprender y compartir las decisiones de tratamiento(7). Por otra parte, la baja adherencia es frecuentemente un problema oculto(5), y puede reflejar un comportamiento intencionado o no, o incluso tener parte de ambos en cuanto al uso o no de un determinado medicamento, un mal uso o incluso un uso elevado(7). En cualquier caso, los estudios muestran una mayor prevalencia de la falta de adherencia intencionada(2).
La baja adherencia de los pacientes es una importante barrera para alcanzar los beneficios clínicos de los medicamentos, que han sido demostrados en ensayos clínicos(7). Estos se realizan entre pacientes voluntarios que son objeto de un seguimiento cercano, que busca garantizar un alto cumplimiento(7). Estos beneficios pueden reducirse o incluso anularse en gran medida en la práctica clínica habitual, donde las tasas de adherencia son bajas(7).
La dificultad de medir
Hay muchos factores posibles relacionados con los medicamentos que pueden influir en la falta de adherencia: complejidad de los regímenes terapéuticos, falta de eficacia, efectos adversos, duración del tratamiento, tratamientos concomitantes, cambios en las prescripciones, fácil acceso a los profesionales de la salud y costos económicos asociados(7).
Sin embargo, medir la falta de adherencia es muy complejo, ya que hay muchos pacientes que toman múltiples tratamientos con diferentes formas de administración(6).
Con el objetivo de intentar comprender las razones para la falta de adherencia y la frecuencia con que se produce, un grupo de investigadores de la Universidad Roseman de Ciencias de la Salud en EEUU, publicó en 2019 un trabajo en el que evaluaba la utilidad de la Escala de Razones para la Adherencia a la Medicación (MAR-Scale)(6).
Se trata de una escala de autoevaluación con 20 ítems. Uno de ellos evalúa la frecuencia global de la falta de adherencia, mientras que los otros 19 evalúan razones frecuentemente mencionadas por los pacientes para la falta de adherencia a la medicación. El desarrollo de esta escala busca alinear los motivos de la falta de adherencia con intervenciones adecuadas para corregirlas(6).
El estudio evaluó la adherencia en 17 enfermedades crónicas. Para medicaciones orales de uso diario, la falta de adherencia fue desde un 25,2% en diabetes a un 63,7% para el eczema. Los motivos más frecuentes para las 17 enfermedades crónicas fueron: “simplemente lo olvidé”, “efectos adversos” y “preocupaciones sobre los efectos a largo plazo”(6).
La situación de los tratamientos de dolor
El dolor crónico no oncológico es un prevalente problema de salud que constituye una carga personal, económica y social que plantea dificultades para su tratamiento(8).
Según un estudio realizado por Sampaio et al. (Facultad de bioimedicina, Universidad de Oporto, Portugal) la falta de adherencia es también común en los pacientes de dolor crónico, más por bajo consumo que por exceso de uso (29,9% vs 13,7%)(5). En contra de la creencia de que principalmente las enfermedades crónicas asintomáticas tienen un impacto negativo en la adherencia, las enfermedades sintomáticas, como el dolor crónico, presentan también tasas de falta de adherencia de alrededor del 50%(5).
En el estudio, la falta de adherencia era del 37% tras 7 días de tratamiento, y aumentó durante los 12 meses de seguimiento hasta alrededor del 50%(5).
Un resultado interesante fue la categorización cualitativa de las razones para la falta de adherencia en función de grupo ACT de medicamentos prescritos para dolor crónico(5). El principal motivo en el caso de los analgésicos antipiréticos fue la falta de eficacia, probablemente por la posibilidad de acceso y consumo sin vigilancia médica, lo que genera desconfianza en su efectividad. En el caso de anti-epilépticos y anti-convulsivos, también la falta de adherencia se debe a creencias sobre falta de eficacia(5). En el otro extremo, los AINE causan gran preocupación sobre sus posibles efectos adversos. La creencia puede resumirse en “menos dolor, más muertes/morbilidad”(5).
Los pacientes con comorbilidades también pueden justificar la falta de adherencia con motivos económicos y retrasar así el inicio de los tratamientos(5). Un aspecto destacado fue que los mayores porcentajes de falta de adherencia se presentaron en los pacientes con síntomas clínicos de depresión(5).
Aunque el estudio no relacionó la intensidad del dolor con la adherencia(5), sí hay trabajos que han incidido en este extremo. Estos trabajos mostraron que hay una pequeña, pero significativa relación inversa entre la adherencia al tratamiento y el control del dolor crónico no oncológico(8).
La influencia de los médicos en la adherencia
Las barreras para la adherencia están relacionadas con el paciente, pero también con el médico(8).
En un trabajo realizado por Margolisy sus colaboradores (Truven Health Analytics, Bethesda, EEUU), se intentó establecer el nivel de adherencia a las guías de tratamiento del dolor en los tratamientos de los pacientes(3). El trabajo se realizó en 5 condiciones crónicas.
Los resultados mostraron que sólo entre un tercio y la mitad de los pacientes son tratados de acuerdo a las guías(3). Entre los motivos podría estar que medir el nivel de dolor es un problema de subjetividad, que puede variar entre los diferentes pacientes y etiologías, complicando el manejo del dolor(3). Además, la mayoría de los pacientes tienen múltiples comorbilidades (frecuentemente psicopatológicas(8)) lo que dificulta determinar con precisión el origen del dolor(3). Otro problema es la posibilidad del uso de opioides, que actualmente puede ser controvertido(3).
La polimedicación dificulta también la adherencia a los tratamientos del dolor, sin embargo, los médicos no la consideraron un problema en más de la mitad de los pacientes(8).
La situación en España
El panorama que comentamos refleja que la adherencia a los tratamientos crónicos es un problema importante, por su impacto en los resultados clínicos, la calidad de vida de los pacientes y en los costes sanitarios(2,6,7). Además es tremendamente complejo. Sus causas pueden estar en la medicación, las comorbilidades, el paciente, los profesionales de la salud o incluso el sistema sanitario, y frecuentemente la falta de adherencia se debe a una combinación de todas las anteriores.
En esta situación, el Observatorio del Dolor realizó en 2019 en España un trabajo de investigación que pretendía establecer los factores asociados a la adherencia a los tratamientos crónicos de dolor comunicados por los pacientes. También pretendía aclarar la frecuencia o importancia de esos factores(2).
El trabajo consistió en una serie de cuestionario rellenados por 1.066 adultos españoles, entre los que 251 (23,5%) sufrían dolor crónico, de los que a 168 (66,9%) se les habían prescrito analgésicos(2).
El primer resultado interesante fue que el 81% de los que tomaban analgésicos decían tomarlos siguiendo las indicaciones del médico. Sin embargo, el 17,6% había olvidado tomar la medicación y el 11% había tomado más medicación de la prescrita(2).
En cuanto a la continuidad del tratamiento, el 46,3% lo abandonó por que se sentía mejor, el 33,3% por empeoramiento y el 7,3% por motivos económicos(2).
En el grupo de personas que comunicaron adherencia al tratamiento, había un mayor porcentaje de personas inactivas, jubiladas o dedicadas a las tareas domésticas que en el grupo de no adherentes. También había más personas tomando más de una medicación (81,7% vs. 57,7%). En cuanto a las medicaciones, más personas adherentes tomaban benzodiacepinas, medicación parenteral o en parches que las no adherentes(2). Esto puede deberse a que estas medicaciones requieren más atención, control e información por parte de los profesionales sanitarios(2).
Por supuesto, los porcentajes de los comportamientos no adherentes siempre eran superiores en el grupo de pacientes que admitían mala adherencia que en el de las personas que se declaraban adherentes: olvidaban más la medicación (34,4% vs 17,6%), suspendían el tratamiento si se encontraban mejor (83,9% frente a 46,3%) o peor (45,2% vs. 33,3%), lo que demuestra una intencionalidad en la falta de adherencia. También olvidaban la medicación a la hora indicada (37,5% vs. 25,7%) o incluso tomaban más medicación si se sentían peor (18,8% vs 11%)(2).
Sin embargo, los problemas económicos parecían afectar más a los pacientes adherentes, pues para el 7,3% de ellos el precio era una causa para abandonar la medicación frente al 3,1% de los no adherentes(2).
Para ambos grupos la atención recibida había sido aceptable, buena o muy buena (91,1% de los pacientes adherentes y 81,3% de los no adherentes), así como la información recibida, que consideraban aceptable, buena o muy buena el 93,4% de los primeros y el 87,5% de los segundos. También ambos grupos se consideraban satisfechos del apoyo de sus familias en un porcentaje elevado (70% y 75% respectivamente)(2).
El estudio evidencia que la mayoría de las personas en tratamiento para el dolor no se comporta de acuerdo a las recomendaciones de su médico(2). Una posible explicación puede ser que la información recibida sea malentendida, olvidada, usada incorrectamente o incluso, completamente ignorada(2).
A pesar de ello, muchos pacientes declaran buena adherencia al tratamiento, quizás porque se considera adecuado socialmente o para ofrecer una imagen de buen paciente(2).
Cerca del 20% de los pacientes habían olvidado tomar la medicación, a pesar de que hasta el momento actual, los olvidos no habían sido considerados una causa de falta de adherencia en pacientes con dolor crónico al tratarse de un síntoma altamente desagradable(2).
Mejorar la adherencia
La clave para mejorar la adherencia a los tratamientos de los pacientes con dolor crónico está en la información.
Es recomendable que los profesionales sanitarios presten atención a la forma en la que comunican a sus pacientes cuál se el comportamiento adecuado para seguir sus recomendaciones de tratamiento(2).
Para los médicos es esencial comprender por qué los pacientes no toman la medicación prescrita(6). Sin embargo, las creencias generales de los pacientes sobre los medicamentos y la adherencia es difícil de establecer(5). Es, por tanto, muy importante animar a los pacientes a expresar su punto de vista sobre los tratamientos ya que esto puede mejorar el cumplimiento(5). De esta manera se podrá identificar antes a los pacientes en alto riesgo de falta de adherencia y desarrollar intervenciones para evitarla(2,5,6).





¿CUÁNTO CUESTA EL DOLOR NEUROPÁTICO?
Ane Mínguez Olaondo (Neuróloga. Hospital Universitario Donostia Osakidetza, Donostia), Alba López Bravo (Neuróloga. Hospital Reina Sofía, Madrid)
El dolor neuropático genera un impacto negativo en la salud física y emocional del paciente, dificulta su desarrollo laboral y social y produce en el sistema un coste económico por gastos de atención sanitaria e incapacidad para trabajar. Una mejora de la eficacia en el manejo del dolor neuropático podría reducir su carga económica.
El dolor es la razón principal por la que los pacientes buscan atención médica, y se ha estimado que genera más de 100 mil millones de dólares por año en costes médicos directos(1). El dolor neuropático (DN) es un tipo específico de dolor crónico causado por “una lesión o enfermedad del sistema nervioso somatosensorial” que puede originarse en el sistema nervioso central o periférico(2). Entre los ejemplos de afecciones en las que el dolor es de origen neuropático se incluyen la esclerosis múltiple, la neuropatía diabética y la neuralgia postherpética.
El 2-3% de la población de los países desarrollados puede desarrollar DN, aunque su prevalencia puede llegar al 7-10% se si utilizan cuestionarios específicos(3).
Este tipo de dolor, por su complejidad, es uno de los mayores desafíos en cuanto al manejo del dolor crónico. En general, el dolor crónico con un componente neuropático se asocia con mayor frecuencia con dolor severo, un mayor número y una mayor gravedad de las comorbilidades, una calidad de vida reducida y unos costes sanitarios globales más elevados(4). El impacto económico de los pacientes con DN es considerable, de forma que, requieren de una alta utilización de recursos de atención sanitaria, como visitas a profesionales médicos y uso de medicamentos.
Diferentes estudios han evaluado los costes directos e indirectos del DN en Europa y Estados Unidos; uno de ellos, analizó la carga económica de pacientes con DN en Francia, Alemania, Italia, Reino Unido y España(5). En España, el coste total (costes directos e indirectos) por paciente fue de 10.597 €, alcanzando los 14.446 € en otros países europeos como Alemania. En nuestro país, los costes sanitarios directos anuales totales por paciente fueron 3.131 € y los costes anuales de los cuidadores ascendieron a 400 €. Con anterioridad, un estudio español mostró como la mayor parte de los costes directos se deben a las hospitalizaciones (45%) y tratamientos farmacológicos (29%), mientras que las visitas médicas y los procedimientos diagnósticos supusieron el 9% y 10% respectivamente(6).
En España, el coste total (costes directos e indirectos) por paciente fue de 10.597 €
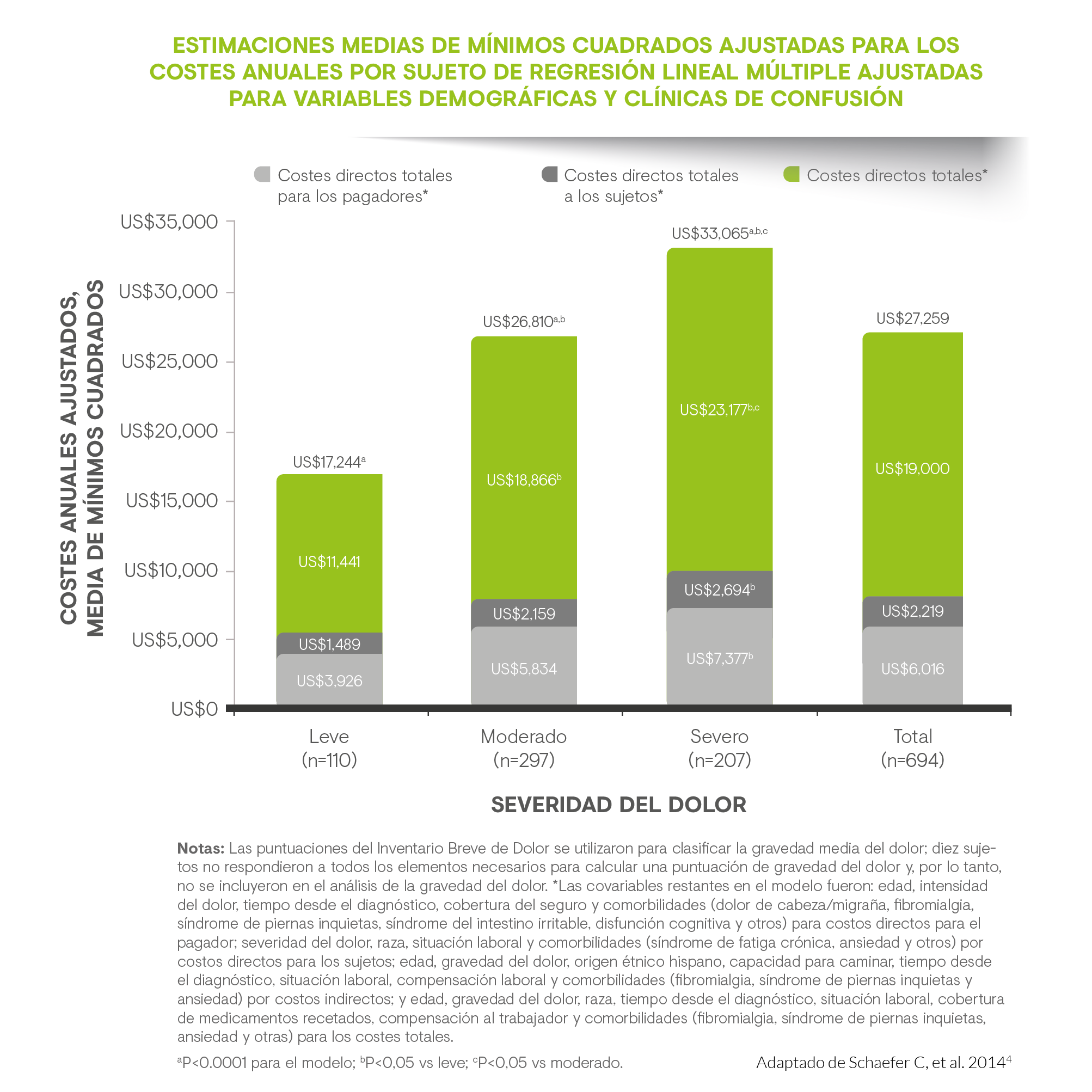
Si nos centramos en la utilización de recursos sanitarios, el más empleado fue el uso de medicamentos (100% de los pacientes), con una media de 2,65 fármacos por paciente. La mayoría de los pacientes tratados en las Unidades del Dolor españolas estaban utilizando fármacos antiepilépticos (87%), opioides (58%) y antidepresivos (36%), mientras que en los pacientes remitidos desde otras especialidades, los tratamientos prescritos previamente fueron los AINE (48%) y opioides (38%). El segundo recurso sanitario empleado con mayor frecuencia por los pacientes españoles fue el tratamiento no farmacológico, seguido de la hospitalización para el control del DN (24,5%), con una media de 22 días de hospitalización(6).
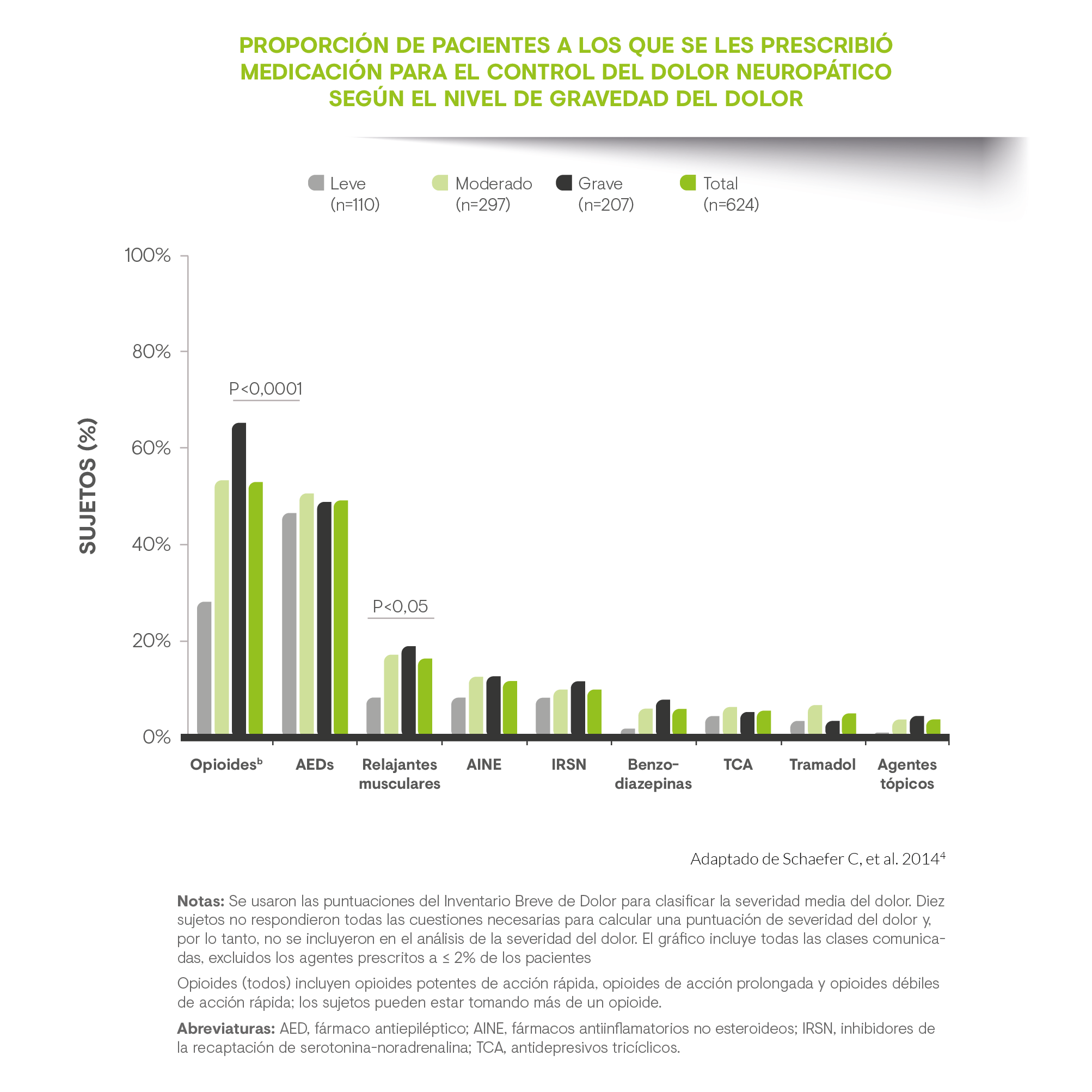
Algunos estudios muestran que dos tercios del coste total son atribuibles a costes indirectos asociados a la discapacidad que conlleva el DN(4). En nuestro país, los costes indirectos debidos a baja por enfermedad ascendieron a 7.066 € y la proporción de pacientes de baja laboral por DN alcanzó el 26% con una media de 11,9 semanas por paciente. De igual manera, la edad media de los pacientes que tuvieron una jubilación anticipada como consecuencia de su DN fue de 52,2 años(5). Así, se ha demostrado que los pacientes con DN tienen un nivel significativamente más bajo de implicación laboral con respecto a personas sin dolor. Además, existe una clara asociación entre DN y mayores tasas de absentismo laboral y una mayor incidencia de problemas de salud que conducen al presentismo(7).
En España los costes indirectos debidos a baja por enfermedad ascienden a 7.066 €
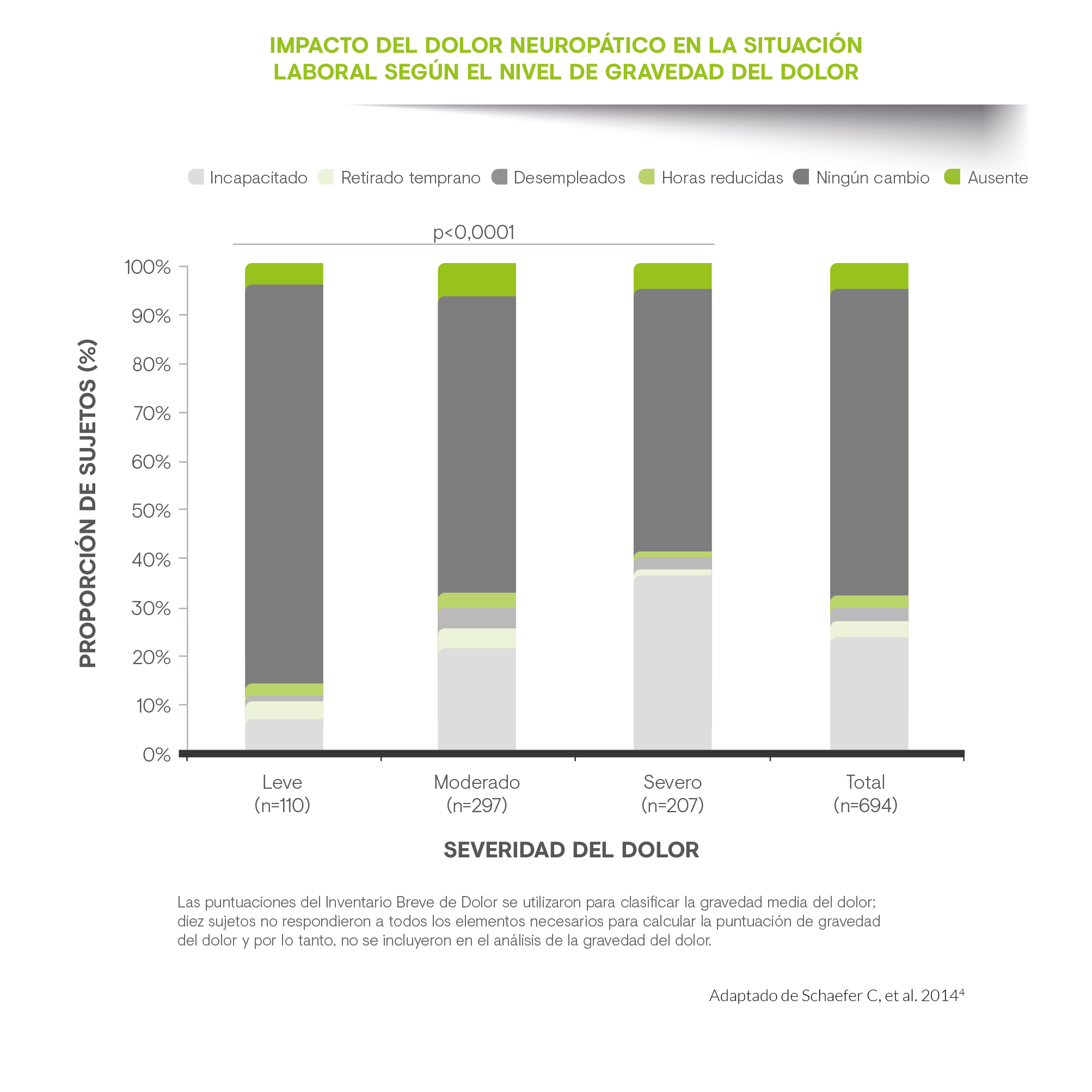
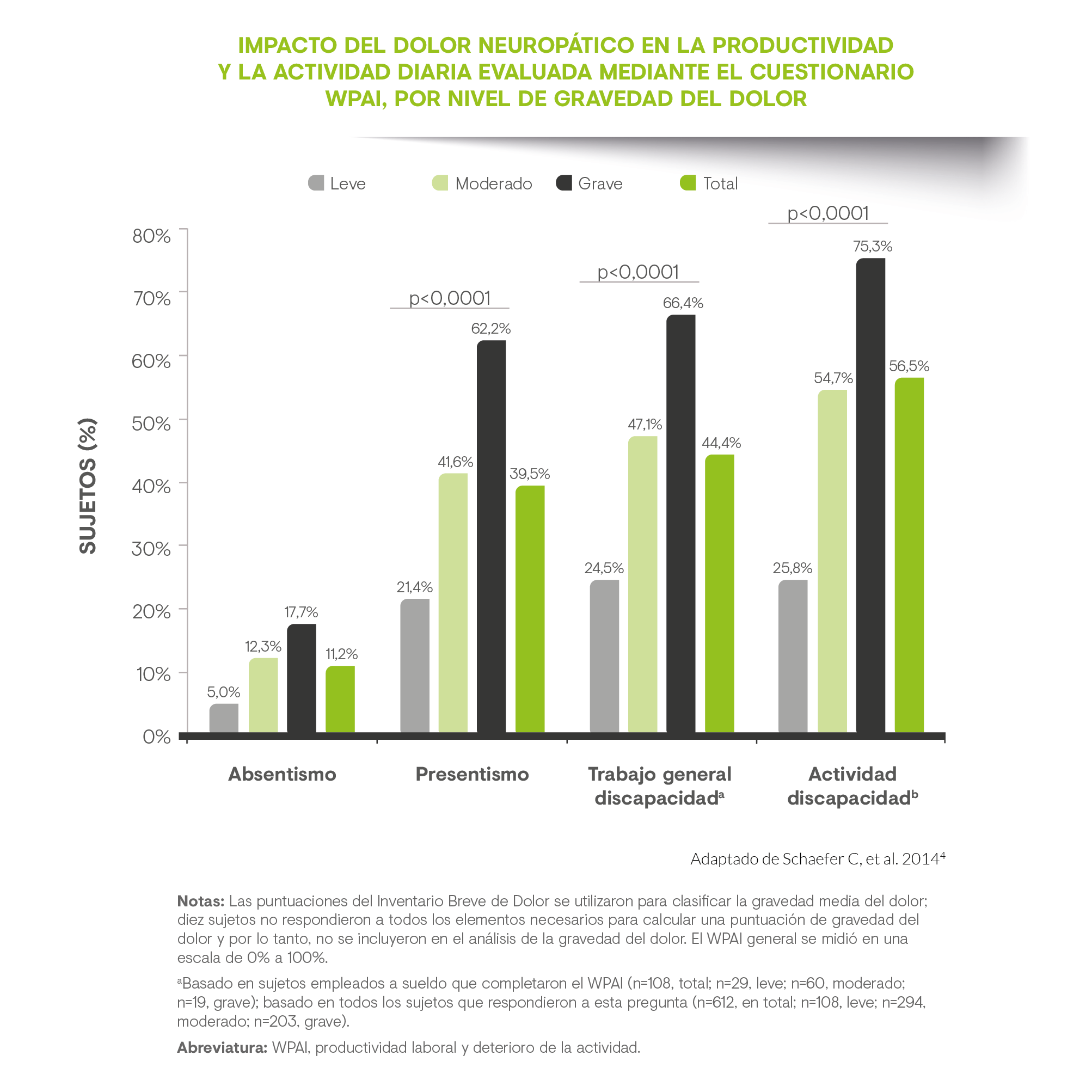
Asimismo, se han analizado los costes del DN según las diferentes etiologías en 18 Unidades del Dolor en España(6), donde las causas más frecuentes fueron: radiculopatías (43,8%), neuralgias (21,2%) y neuropatías (10,5%). Dentro de las radiculopatías, la más frecuente fue la lumbosacra (34,6%) seguida de la cervical (8,6%). Las causas más frecuentes de neuralgia fueron la neuralgia postherpética (11,3%) y la neuralgia del trigémino (6,9%).
A modo de ejemplo, la neuralgia postherpética genera un mayor número de visitas a Atención Primaria, pérdidas de productividad laboral y costes sanitarios(8). Lo mismo ocurre con la neuralgia del trigémino, en la que el dolor tiene un impacto directo en la utilización de recursos médicos, de modo que casi el 80% de los pacientes afirma haber visitado a su médico al menos una vez en el último mes. Además, el dolor asociado a esta patología afecta al 34% de los pacientes en el ámbito laboral, con una media de 3,9 días perdidos en el trabajo en el mes anterior, según datos de un estudio realizado en seis ciudades europeas(9). Igualmente, los pacientes con DN asociado a una lesión medular muestran una funcionalidad deficiente y una pérdida de productividad laboral(10).
De esta forma, el dolor neuropático puede afectar sustancialmente a la calidad de vida, ya que a menudo se asocia con otros problemas, como la pérdida de la funcionalidad, la presencia de ansiedad, depresión, trastornos del sueño, insatisfacción sexual e incluso fallos subjetivos de memoria y deterioro cognitivo, al igual ocurre en el dolor crónico(11-13). Por ello, cada vez se da más valor al impacto de las afecciones que conllevan dolor en las actividades diarias, así como en el funcionamiento físico, mental, emocional y social tanto de la persona que lo padece como de su entorno(14).
Con el objetivo de cuantificar este efecto, se utilizan diferentes herramientas para evaluar la eficacia de las intervenciones realizadas en los pacientes con DN. La mayoría de las herramientas para evaluar la calidad de vida son genéricas pero también las hay específicas(15). Ejemplo de ello, son las encuestas de salud como el formulario corto de 36 ítems (SF-36), el perfil de salud de Nottingham(16) o el EQ-5D. Como cuestionario más específico, cabe destacar el NeuroQol, un instrumento específicamente validado para neuropatía y úlcera de pie(17,18). En relación a esto, los estudios realizados han demostrado que la discapacidad causada por la neuropatía se correlaciona con una disminución de la calidad de vida, y que la neuropatía dolorosa se asocia con una peor calidad de vida en comparación con la indolora, independientemente de la causa(19).
CONCLUSIONES
El dolor neuropático tiene un efecto devastador en muchos aspectos de la vida diaria, de forma que no sólo disminuye la calidad de vida del paciente al repercutir negativamente en su salud física y emocional. También tiene efectos adversos en ámbitos no relacionados con la salud ya que dificulta participar plenamente de la vida social y familiar. Además, desde el punto de vista económico, el DN genera gastos debidos a la atención sanitaria y disminuye considerablemente la capacidad para trabajar de manera productiva. La magnitud de los costes directos e indirectos en los pacientes con DN sugiere que una mejora de la eficacia en el manejo del dolor podría reducir su carga económica. Dado que la calidad de vida se ve afectada en pacientes con DN debido a la toma de fármacos, así como las visitas médicas y la morbilidad asociada a la propia enfermedad, un diagnóstico y tratamiento certero y rápido repercutirá en una mejor calidad de vida del paciente y en un ahorro en la carga económica de esta enfermedad.



Una nueva herramienta para médicos rurales
SEMERGEN y GRÜNENTHAL se unen en la creación de la plataforma: www.gen-rural.es, una nueva herramienta que ofrece un programa de actualización científica personalizada a los médicos de AP que desarrollan su actividad diaria en el medio rural.
GEN-RÜRAL es una iniciativa de la Sociedad Española de Médicos de Atención Primaria (SEMERGEN) que cuenta con el apoyo de Grünenthal. Su objetivo: ofrecer al 7% de médicos que en España desarrolla su actividad clínica en municipios de menos de 5.000 habitantes1, un completo programa de actualización científica.
El proyecto, presentado en el I Congreso de Medicina Rural de SEMERGEN celebrado los pasados días 21 al 24 de junio, cuenta con la web www.gen-rural.es como medio de acceso a esta información.
La situación pandémica actual, ha potenciado también en el medio rural el acceso a la información y la conectividad de manera online. El objetivo de GEN-Rüral es potenciar esta conectividad y utilizarla como palanca para que el médico rural acceda a la formación personalizada en el manejo del dolor crónico. “Nuestro origen como sociedad científica está muy vinculado a la medicina rural. Por ello hemos puesto en marcha este proyecto que pretende estar más cerca de los médicos que ejercen en zonas rurales y dar respuesta a la demanda de estos profesionales de recibir herramientas y formación para abordar mejor el dolor crónico”, explica el Dr. Javier Sanz, coordinador del grupo de trabajo de Nuevas Tecnologías de SEMERGEN y responsable de este proyecto.
La extensión de la tecnología en las áreas rurales no es la única oportunidad en la que se basa este proyecto. GEN-RÜRAL también busca apoyarse en la atención de la opinión pública y las instituciones que por fin ha llegado a la España vaciada y que se expresa –entre otras iniciativas– en el plan del Gobierno con 136 medidas para revertir los efectos de la despoblación y el éxodo rural y que está financiado con 10.000 millones de euros del fondo de recuperación europeo.
¿Qué puede encontrar en GEN-RÜRAL?
La plataforma GEN-RURAL ofrece un completo programa de actualización científica con información médica, cursos online, webinars y recursos para los pacientes.
¿A quién va dirigido GEN-RURAL?
Pueden acceder y hacer uso de esta plataforma de forma gratuita, todos los profesionales de la salud que desarrollen su actividad en municipios del medio rural.
El dolor crónico en las áreas rurales
Las enfermedades que cursan con dolor crónico son muy prevalentes en estas áreas rurales debido, en gran parte, al envejecimiento de la población. De ahí que la atención de esta circunstancia cobre especial relevancia en este tipo de entornos.
Además, la COVID-19 ha aumentado el dolor en más del 57,4% de las personas que padecen dolor crónico(1). Todo ello implica necesidades de formación, reciclaje profesional y apoyo para los médicos rurales a las que este plan piloto busca dar respuesta.
(1) Resultados encuesta paciente dolor crónico y Covid-19. [Internet]. Madrid: Sociedad Española del Dolor (SED). Junio, 2020. [Citado 25 may 2021].







DIAGNOSTIC TOOL
Herramienta que facilita el diagnóstico del Dolor Neuropático Localizado durante el ejercicio profesional
Uni2 talks •
A PODCAST ON ANCHOR
Conversando sobre los nuevos retos en dolor crónico.
Entrevistas en torno a los retos asistenciales post COVID-19: telemedicina, asistencia remota, atención domiciliaria, digitalización de los servicios sanitarios,..
Producido por Grünenthal España.














